|
© Borgis - Postępy Nauk Medycznych 8, s. 610-613
*Michał Pirożyński
Niedodma: patofizjologia, objawy kliniczne
Pulmonary atelectasis: pathophysiology, clinical signs
Klinika Anestezjologii i Intensywnej Terapii Centrum Medycznego Kształcenia Podyplomowego
Kierownik Kliniki: prof. dr. hab. med. Jacek Jastrzębski Streszczenie
Termin niedodma obejmuje szereg schorzeń, których wspólnym elementem jest utrata powietrza przez miąższ płucny, a zarazem zmniejszona objętość tego obszaru. Należy pamiętać, że zmniejszeniu objętości nie musi towarzyszyć zmiana przejrzystości, zatem w badaniu radiologicznym niedodmie nie musi towarzyszyć zmniejszona przejrzystość obszaru płuc. Najczęściej występuje niedodma resorpcyjna lub niedodma obturacyjna spowodowana obecnością wewnątrzoskrzelowej przeszkody lub uciskiem oskrzela z zewnątrz. W zdrowym miąższu płucnym całkowita resorpcja gazów z dróg oddechowych i pęcherzyków płucnych następuje w przeciągu 18-24 godzin od pojawienia się czynnika zamykającego oskrzele. Niedodma kompresyjna powstaje na skutek ucisku przez powietrze lub płyn gromadzący się w jamach opłucnej. Wielkość niedodmy jest wprost proporcjonalna do objętości płynu lub powietrza uciskającego miąższ płucny, pod warunkiem braku zrostów w jamie opłucnowej. Przy odmie całkowitej płuco o objętości około 3,5 L zajmuje objętość wielkości piłki tenisowej. Autorzy omawiaja przyczyny oraz objawy różnych postaci niedodmy. Słowa kluczowe: niedodma, patofizjologia, zatorowość płucna
Summary
The term atelectasis encompasses several disorders, but its common sign is loss of volume of the pulmonary parenchyma. The loss of volume of the parenchyma does not mean the loss of translucency that can be appreciated on a chest radiogram. The most common form of atelectasis is resorptional or obstructional atelectasis caused by an obstacle in the draining airway. In a healthy lung the complete loss of air within can occur 18-24 hours following the onset of the acute obstruction factor. Compression atelectasis is caused by a facor (fluid or air) that is present in the pleural cavity and grow in volume casing compression of the underlying parenchyma. The size of the atelectasis is governed by the volume of air or fluid that causes the compression. In a full atelectasis of the lung, the lung that normally has a volume of 3.5 L is shrunken to the size of a tennis ball. The authors discuss the pathophysiology, and signs of various forms of atelectasis. Key words: atelectasis, pathophysiology, pulmonary thromboembolism
Termin niedodma obejmuje szereg schorzeń, których wspólnym elementem jest utrata powietrza przez miąższ płucny, a zarazem zmniejszona objętość tego obszaru. Należy pamiętać, że zmniejszeniu objętości nie musi towarzyszyć zmiana przejrzystości, zatem w badaniu radiologicznym niedodmie nie musi towarzyszyć zmniejszona przejrzystość obszaru płuc. Dowodem tego jest zatorowość płucna, której towarzyszy znaczne zmniejszenie objętości miąższu, a jedynym dowodem będzie uniesienie kopuły przepony.
Płuca posiadają naturalną tendencję zapadania się. Temu zjawisku sprzeciwiają się siły rozciągania klatki piersiowej. Z chwilą utraty działania tych sił (np. na skutek odmy opłucnowej) dochodzi do powstania biernej niedodmy i zapadnięcia się miąższu płucnego (w tym przypadku nawet całego płuca lub tylko jednego jego fragmentu).
W przypadku rosnącej sztywności miąższu płucnego (gdy podatność maleje), objętość maleje. Przykładem takiego stanu jest włóknienie płuc, a niedodma określana jest mianem bliznowatej (ang. cicatrization atelectasis). Zaburzenia w czynności surfaktantu prowadzą do zapadania się pęcherzyków płucnych, a niedodma bywa określana mianem mikroniedodmy lub niedodmy ogniskowej.
Najczęściej występuje niedodma resorpcyjna lub niedodma obturacyjna spowodowana obecnością wewnątrzoskrzelowej przeszkody lub uciskiem oskrzela z zewnątrz. W zdrowym miąższu płucnym całkowita resorpcja gazów z dróg oddechowych i pęcherzyków płucnych następuje w przeciągu 18-24 godzin od pojawienia się czynnika zamykającego oskrzele (1). Zamknięcie dopływu powietrza w oskrzelu nie zawsze skutkuje niedodmą, a to z powodu rozwijania się obocznej wentylacji (2).
Niedodma kompresyjna powstaje na skutek ucisku przez powietrze lub płyn gromadzący się w jamach opłucnej. Wielkość niedodmy jest wprost proporcjonalna do objętości płynu lub powietrza uciskającego miąższ płucny, pod warunkiem braku zrostów w jamie opłucnowej. Przy odmie całkowitej płuco o objętości około 3,5 L zajmuje objętość wielkości piłki tenisowej.
Cechą charakterystyczną niedodmy biernej (pasywnej) jest utrata objętości w regionach najniżej położonych (najczęściej w segmentach podstawnych obu dolnych płatów, a u leżącego w segmentach tylnych górnych i dolnych płatów). Najczęściej mamy do czynienia z bierną niedodmą u chorych poddawanych długiemu znieczuleniu, we wczesnym okresie pooperacyjnym (ryc. 1) (3). Zmiany takie spotykamy zwłaszcza u chorych z obrzękiem płuc, zwiększoną objętością krążącej krwi, zaburzeniami transportu śluzowo-rzęskowego, u palaczy tytoniu na skutek zaburzeń budowy drobnych oskrzeli (4, 5, 6).
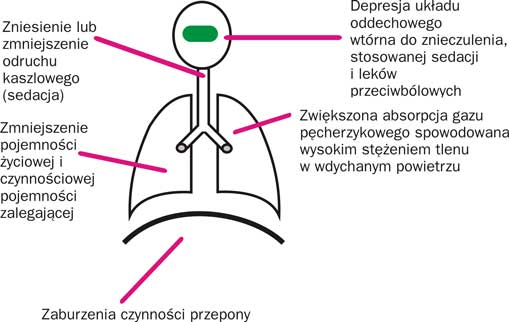 Ryc. 1. Przyczyny niedodmy pooperacyjnej.
Niedobór czynnika powierzchniowego lub jego zaburzenia czynnościowe są przyczyną ogniskowej niedodmy. Zmiany te spotyka się w przebiegu ARDS, zespołu błon szklistych lub zmian popromiennych (6). Uważa się, że ten typ niedodmy bywa również spotykany w okresie pooperacyjnym (7, 8).
Włóknienie obszaru niedodmowego lub pojawienie się zmian marskich wiążą się z utratą objętości obszaru płuc rzadko, jednak spostrzegane są jako zmiany niedodmowe, choć w piśmiennictwie anglosaskim bywają określane mianem niedodmy bliznowatej. Podstawą zachodzących zmian są procesy włóknienia, które prowadzą do znacznej utraty objętości miąższu płucnego. Zmiany radiologiczne mogą być zlokalizowane ale również uogólnione.
Zmiany zlokalizowane spotykamy w przebiegu schorzeń ziarniniakowatych np. w przebiegu gruźlicy. Z powodu wzrostu skoku sprężystego u tych chorych dochodzi do powstawania zaburzeń w budowie oskrzeli z pociągania ścian przez zmiany bliznowate (tzw. rozstrzenie z pociągania) (9). Towarzyszące temu zmiany radiologiczne to zmniejszenie objętości segmentu lub płata, z niejednorodnymi obszarami niedodmy i przejaśnień, zmianami zagęszczeń od zmian niedodmowych do wnęk (ryc. 2). Zmiany niedodmowe mogą być tak zaawansowane, że na zwykłym zdjęciu radiologicznym cały segment może nie być widoczny (dotyczy to zwłaszcza segmentów szczytowych).
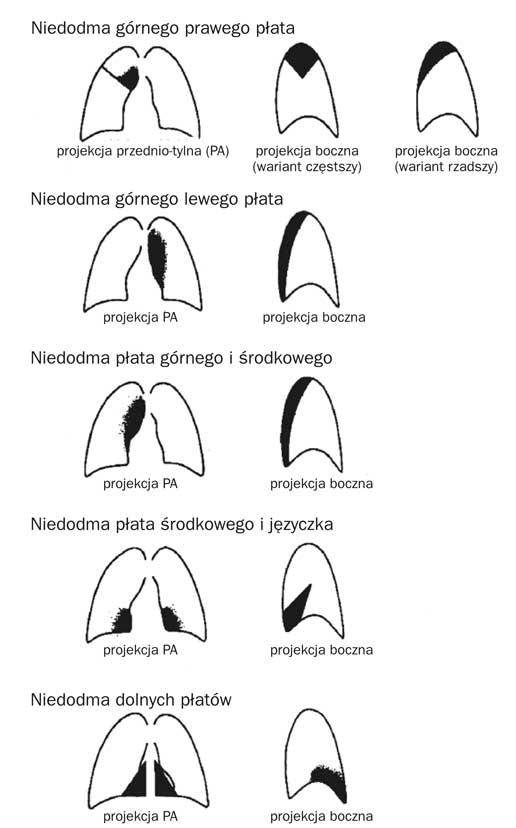 Ryc. 2. Najczęściej spotykane obrazy radiologiczne niedodmy.
Zmiany radiologiczne niedodmy mogą być bezpośrednie (przemieszczenie szczelin międzypłatowych, zagęszczenie rysunku naczyń i oskrzeli) oraz pośrednie (zmiany gęstości rysunku, przemieszczenie struktur anatomicznych) (tab. 1).
Tabela 1. Radiologiczna cechy niedodmy.
Cechy radiologiczne niedodmy po raz pierwszy zostały opisane w 1945 roku (10, 11, 12, 13, 14, 15). Na charakterystyczne zmiany niewątpliwie mają wpływ współistniejące zmiany chorobowe w układzie oddechowym. Rutynowe badania klatki piersiowej nie zawsze umożliwiają wykrycie przyczyn zmian niedodmowych. Badanie tomografii komputerowej ułatwia wykrycie przyczyny powstania niedodmy. Pozwala również na dokładniejszą ocenę obszaru niedomowego.
Niedodma obejmująca całe płuco spowodowana jest najczęściej ograniczeniem przepływu powietrza przez główne oskrzele (np. przez guz, ale również zalegającą gęstą wydzielinę).
Zmiany niedodmowe płatów różnią się w zależności od lokalizacji (ryc. 2). Przyczynami mogą być nie tylko zmiany egzofityczne oskrzeli, ale również i zmiany zapalne. Zmiany niedodmowe segmentów płuc najczęściej spowodowane są zmianami zapalnymi.
Najczęściej występującymi zmianami są tzw. płytki niedodmowe, widoczne u podstaw obu płuc (linie Fleischnera). Przyczyną tych zmian są najczęściej: wadliwa czynność przepony, utrudniony odruch kaszlowy (w okresie pooperacyjnym), utrudniona ewakuacja płynu z obwodowych dróg oddechowych oraz zaburzona czynność surfaktantu. Zmiany te bywają również spostrzegane w zatorowości płucnej. Dlatego stwierdzenie takich zmian w obrazie radiologicznym klatki piersiowej powinno wzmóc czujność diagnostyczną lekarza.
Piśmiennictwo
1. COULTER WW, Jr. Experimental massive pulmonary collapse. Dis Chest 1950 August; 18 (2): 146-53.
2. Culiner MM, REICH SB: Collateral ventilation and localized emphysema. Am J Roentgenol Radium Ther Nucl Med 1961 February; 85: 246-52.
3. Strandberg A et al.: Densities in dependent lung regions during anaesthesia: atelectasis or fluid accumulation? Acta Anaesthesiol Scand 1986 April; 30 (3): 256-9.
4. Gamsu G et al.: Postoperative impairment of mucous transport in the lung. Am Rev Respir Dis 1976 October; 114 (4): 673-9.
5. Remy-Jardin M et al.: Morphologic effects of cigarette smoking on airways and pulmonary parenchyma in healthy adult volunteers: CT evaluation and correlation with pulmonary function tests. Radiology 1993 January; 186 (1): 107-15.
6. Woodring JH, Reed JC: Types and mechanisms of pulmonary atelectasis. J Thorac Imaging 1996; 11 (2): 92-108.
7. Benjamin JJ et al.: Left lower lobe atelectasis and consolidation following cardiac surgery: the effect of topical cooling on the phrenic nerve. Radiology 1982 January; 142 (1): 11-4.
8. Wilcox P et al.: Phrenic nerve function and its relationship to atelectasis after coronary artery bypass surgery. Chest 1988 April; 93 (4): 693-8.
9. Westcott JL, Cole SR: Traction bronchiectasis in end-stage pulmonary fibrosis. Radiology 1986 December; 161 (3): 665-9.
10. BUTZ GW, Jr., AMORY HI: Atelectasis: its diagnosis and significance. W V Med J 1963 July; 59: 183-9.
11. Duggan M, Kavanagh BP: Atelectasis in the perioperative patient. Curr Opin Anaesthesiol 2007 February; 20 (1): 37-42.
12. Jones JR, Fieber WW: Current concepts in atelectasis. Med Times 1966 January; 94 (1): 48-50.
13. Katz S: Linear atelectasis. GP 1957 August; 16 (2): 108-9.
14. Stathopoulos GT et al.: Rounded atelectasis of the lung. Respir Med 2005 May; 99 (5): 615-23.
15. Tsai KL, Gupta E, Haramati LB: Pulmonary atelectasis: a frequent alternative diagnosis in patients undergoing CT-PA for suspected pulmonary embolism. Emerg Radiol 2004 April; 10 (5): 282-6.
otrzymano/received: 2009-04-29 zaakceptowano/accepted: 2009-07-01 Adres/address: *Michał Pirożyński Klinika Anestezjologii i Intensywnej Terapii CMKP ul. Czerniakowska 231, 00-416 Warszawa tel.: (0-22) 825-03-52 e-mail: kl.anestezjologii@szpital-orlowskiego.pl Pełna wersja artykułu Niedodma: patofizjologia, objawy kliniczne dostępna w Czytelni Medycznej Borgis. |
||||||||||||||||||||||
Chcesz być na bieżąco? Polub nas na Facebooku: strona Wydawnictwa na Facebooku |








