|
© Borgis - Postępy Nauk Medycznych 9, s. 615-621
Krzysztof Czyżewski, *Jan Styczyński, Robert Dębski, Anna Krenska, Mariusz Wysocki
Zastosowanie paliferminu u dzieci i młodzieży poddawanych transplantacji allogenicznych komórek krwiotwórczych
Palifermin use in children and adolescents undergoing allogeneic hematopoietic stem cell transplantation
Katedra Pediatrii, Hematologii i Onkologii, Collegium Medicum im. L. Rydygiera, Uniwersytet Mikołaja Kopernika, Bydgoszcz
Kierownik Katedry: prof. dr hab. med. Mariusz Wysocki Szpital Uniwersytecki nr 1 im. Jurasza, Bydgoszcz Dyrektor Szpitala: mgr inż. Jacek Kryś Streszczenie
Wstęp. Palifermin, rekombinowany ludzki czynnik wzrostu keratynocytów, zmniejsza ryzyko wystąpienia zapalenia śluzówek jamy ustnej u dorosłych pacjentów poddawanych transplantacji komórek krwiotwórczych. Aktualne dowody naukowe wskazują, że u pacjentów dorosłych palifermin skraca również czas żywienia pozajelitowego i czas hospitalizacji, a także zmniejsza użycie leków narkotycznych do kontroli bólu wywołanego zapaleniem śluzówek. Cel pracy. Celem pracy jest prospektywna analiza bezpieczeństwa i skuteczności zastosowania paliferminu u dzieci i młodzieży. Materiał i metody. Do analizy włączono 79 kolejnych pacjentów, poddanych transplantacji allogenicznych komórek krwiotwórczych, u których zastosowano palifermin. Analizę skuteczności leku przeprowadzono w odniesieniu do grupy 32 pacjentów, u których nie stosowano paliferminu. Wyniki. Palifermin zmniejszał ryzyko wystąpienia ciężkiego zapalenia śluzówek jamy ustnej, ostrej choroby przeszczep przeciwko gospodarzowi (≥ 2 stopień), przewlekłej postaci choroby przeszczep przeciwko gospodarzowi oraz konieczność użycia morfiny w łagodzeniu bólu wywołanego zapaleniem śluzówek jamy ustnej. Użycie paliferminu nie wpływało natomiast na skrócenie czasu żywienia pozajelitowego. Spośród 79 pacjentów otrzymujących palifermin, jedynie u jednego obserwowano objawy niepożądane pod postacią uogólnionego rumienia i świądu całego ciała. Natomiast wyniki uzyskane w poszczególnych podgrupach w zależności od typu dawcy (rodzinny vs alternatywny) lub zastosowanego kondycjonowania (chemioterapia vs oparte na TBI) osiągnęły różny poziom istotności statystycznej wynikający najprawdopodobniej z liczebności podgrup. Wnioski. Palifermin jest bezpiecznym lekiem stosowanym u dzieci i młodzieży poddanych transplantacji allogenicznych komórek krwiotwórczych. Zastosowanie tego leku wiąże się z istotnym zmniejszeniem powikłań związanych z uszkodzeniem błon śluzowych oraz zmniejszeniem ryzyka rozwoju ostrej i przewlekłej choroby GVHD. Słowa kluczowe: palifermin, zapalenie śluzówek jamy ustnej, transplantacja allogenicznych komórek krwiotwórczych, choroba przeszczep przeciwko gospodarzowi
Summary
Introducton. Palifermin, a recombinant human keratinocyte growth factor, is used in adults to prevent oral mucositis following allogeneic stem cell transplantation. Palifermin decreases total parenteral nutrition, length of initial hospital stay and opioid usage in pain control caused by oral mucositis in adults. Aim. The objective of this prospective study was the analysis of safety and efficacy of palifermin in children and adolescents. Material and methods. Seventy-nine consecutive patients undergoing allogeneic stem cell transplantation and treated with palifermin were included into the study. The results of efficacy were compared to data of 32 patients, not treated with palifemin. Results. Palifermin decreased incidence of severe oral mucositis (grade 3 and 4 WHO), acute graft versus host disease (≥ 2 grade), chronic graft versus host disease, and opioid usage in pain control caused by oral mucositis. Palifermin did not affect time of total parenteral nutrition. Adverse events of palifermin use were observed only in one patient as generalized itch and erythema. Data obtained in particular subgroups: type of donor (sibling vs alternative) or type of conditioning (chemotherapy vs TBI-based) reached different statistical significance level, what was limited by number of patients in particular subgroups. Conclusions. Palifermin is a safe drug when used in children and adolescents undergoing allogeneic stem cell transplantation. The use of this drug leads to significant decrease of mucosal toxicity and frequency of acute and chronic GVHD. Key words: palifermin, mucositis, allogeneic stem cell transplantation, graft versus host disease
Wstęp
Zapalenie śluzówek jamy ustnej (ang. oral mucositis – OM) jest jednym z najczęstszych powikłań leczenia przeciwnowotworowego (1). U pacjentów poddawanych przeszczepieniu komórek krwiotwórczych (ang. hematopoietic stem cell transplantation – HSCT) terapia wysokodawkowa z zastosowaniem chemio-/radioterapii może powodować OM do 100% pacjentów (2). OM rozpoczyna się najczęściej 3 do 10 dni od początku chemioterapii i może się utrzymywać do trzech tygodni od jej zakończenia (3). Szczyt występowania OM obserwuje się najczęściej pomiędzy 6 a 12 dniem po transplantacji, natomiast ustępowanie objawów OM pomiędzy 14 a 18 dniem po transplantacji (4). Czynniki ryzyka występowania OM nie zostały dotychczas jednoznacznie określone (3, 4). Jednakże zastosowanie całkowitego napromienienia ciała (ang. total body irradiation – TBI), metotreksatu, etopozydu, fluorouracylu, bleomycyny, doksorubicyny, paklitakselu znamiennie podnosi ryzyko wystąpienia OM (3, 4).
Większość dzieci poddawanych chemioterapii doświadcza różnego stopnia OM, a częstość występowania oraz stopień nasilenia OM zależą od rodzaju nowotworu i zastosowanego leczenia przeciwnowotworowego (5). W chwili obecnej nie ma jednego protokołu postępowania w zapobieganiu OM, a zastosowanie różnych środków działających miejscowo ma ograniczoną skuteczność (3, 6).
OM jest związane z uszkodzeniem błony śluzowej o charakterze łagodnego zaniku do ciężkich owrzodzeń powodujących ból uniemożliwiający połykanie śliny, płynów i pokarmów (7, 8). OM sprzyja zakażeniom florą oportunistyczną pacjentów, przyczyniając się do rozwoju ciężkich zakażeń, posocznicy, choroby przeszczep przeciwko gospodarzowi (ang. graft-versus-host disease – GVHD), a także do wydłużeniu czasu hospitalizacji oraz zwiększenia kosztów leczenia (6, 8). Występowanie OM może się wiązać ze wzrostem ryzyka śmiertelności (3, 6).
Czynnik wzrostu keratynocytów (ang. keratinocyte growth factor – KGF) jest pierwszym opisanym czynnikiem wzrostu komórek nabłonkowych, wykazującym działanie protekcyjne w stosunku do uszkodzenia spowodowanego chemio- lub radioterapią (3, 9). Palifermin, ludzki rekombinowany czynnik wzrostu keratynocytów, w sposób swoisty stymuluje wzrost oraz działa antyapoptotycznie na komórki nabłonkowe wykazujące obecność receptora dla KGF na swojej powierzchni. Równocześnie nie działa na komórki, które tego receptora nie posiadają. Wykazano znaczącą skuteczność tego leku u dorosłych w redukcji uszkodzenia śluzówek błony śluzowej jamy ustnej i innych odcinków przewodu pokarmowego, wywołanych chemio- lub radioterapią (9). Dobra skuteczność i wysoki profil bezpieczeństwa paliferminu został wielokrotnie wykazany u dorosłych pacjentów poddawanych transplantacji komórek krwiotwórczych. Natomiast dane dotyczące zastosowania paliferminu u dzieci i młodzieży poddawanych HSCT są ograniczone (3).
Cel pracy
Celem tej pracy jest prospektywna analiza bezpieczeństwa i skuteczności zastosowania paliferminu u dzieci i młodzieży.
Materiał i metody
Badaniem objęto łącznie 111 pacjentów poddanych w latach 2003-2012 allogenicznej transplantacji komórek krwiotwórczych w Oddziale Transplantacji Szpiku Kostnego Kliniki Pediatrii, Hematologii i Onkologii Szpitala Uniwersyteckiego nr 1 w Bydgoszczy. Do grupy badanej włączono 79 kolejnych pacjentów, u których zastosowano palifermin. Analizę skuteczności leku przeprowadzono w odniesieniu do grupy 32 pacjentów, u których nie stosowano paliferminu. Charakterystykę pacjentów podano w tabeli 1.
Rekombinowany czynnik wzrostu keratynocytów, palifermin (Kepivance, Amgen, Breda, Holandia) stosowano przed kondycjonowaniem i po nim, w jednej dawce 60 μg/kg dożylnie przez trzy kolejne dni (łącznie 6 dawek).
Podczas hospitalizacji każdy pacjent otrzymujący palifermin był codziennie oceniany pod kątem: działania niepożądanego paliferminu, stopnia zapalenia śluzówek jamy ustnej, ostrej postaci choroby przeszczep przeciwko gospodarzowi (ang. acute graft-versus-host disease – aGVHD). Występowanie i nasilenie ostrej i przewlekłej postaci choroby przeszczep przeciwko gospodarzowi (ang. chronic graft-versus-host disease – cGVHD) oceniano każdorazowo podczas wizyty w poradni transplantacji szpiku kostnego lub podczas hospitalizacji. OM oceniano w pięciostopniowej skali WHO (3, 10) od rozpoczęcia kondycjonowania do czasu wypisu do domu lub zgonu pacjenta. W analizie wzięto pod uwagę również konieczność użycia morfiny w łagodzeniu objawów OM, a także czas stosowania żywienia pozajelitowego (ang. total parenteral nutrition – TPN). Stopień nasilenia aGVHD oceniano wg standardowej skali (11), a w razie potrzeby wykonywano biopsję narządu objętego procesem chorobowym. Stopień nasilenia cGVHD oceniono za pomocą badania klinicznego, badań laboratoryjnych lub biopsji narządu podejrzanego o zajęcie GVHD (12).
U wszystkich pacjentów stosowano standardowe postępowanie związane z kondycjonowaniem i leczeniem wspomagającym. W zależności od rozpoznania, profilaktyka choroby przeszczep przeciwko gospodarzowi obejmowała podawanie cyklosporyny i metotreksatu (n = 83; 74,4%), cyklosporyny (n = 20; 18,0%), cyklosporyny, metotreksatu i rytuksymabu (n = 5; 4,5%), cyklosporyny i metyloprednizonu (n = 2; 1,8%) lub cyklosporyny i mykofenolanu mofetylu (n = 1; 0,9%). U 69 (62,1%) pacjentów zastosowano dodatkowo globulinę antytymocytarną (ATG), a u 3 (2,7%) alemtuzumab.
U wszystkich pacjentów zastosowano profilaktykę przeciwinfekcyjną w oparciu o ciprofloksacynę lub aksetyl cefuroksymu, flukonazol, acyklowir, trimetoprim/sulfometaksazol. We wczesnym okresie poprzeszczepowym, 2 razy w tygodniu monitorowano EBV-DNA i CMV-DNA-emię metodą PCR.
Analiza statystyczna
Cechy niekategoryczne porównano testem Manna--Whitneya, a cechy kategoryczne testem chi-kwadrat, określając jednocześnie iloraz szans (ang. odds ratio – OR) z 95% przedziałem ufności (ang. confidence interval – CI). Krzywe przeżycia wolnego od choroby (ang. disease free survival – DFS) oraz całkowitego przeżycia (ang. overall survival – OS) wyznaczono metodą Kaplana-Meiera i porównano testem log-rank. Za istotne statystycznie uznano p ≤ 0,05. Analizę przeprowadzono, stosując pakiet statystyczny SPSS21.
Wyniki
Porównanie płci, wieku i masy ciała pacjentów, u których zastosowano palifermin i go nie zastosowano, nie wykazało istotnych statystycznie różnic pomiędzy grupami (tab. 1). W obu analizowanych grupach nie wykazano również istotnych statystycznie różnic w użyciu kondycjonowania mieloablacyjnego (ang. myeloablative conditioning regimen – MAC) i o zredukowanej toksyczności (ang. reduced intensity conditioning regimen – RIC), a także w stosowaniu w kondycjonowaniu samej chemioterapii (CHT) lub połączenia całkowitego napromieniowaniem ciała (ang. total body irradiation – TBI) z CHT. U pacjentów, dla których dawcą było rodzeństwo zgodne w HLA (ang. matched family donor – MFD), częściej nie stosowano paliferminu, natomiast u pacjentów poddanych transplantacji od dawcy alternatywnego palifermin był stosowany znamiennie częściej. Większość transplantacji w pierwszych pięciu latach działalności ośrodka była przeprowadzona bez użycia paliferminu, natomiast w kolejnych latach, transplantacje odbywały się głównie z zastosowaniem tego leku.
Tabela 1. Charakterystyka pacjentów.
ALL – ostra białaczka limfoblastyczna, AML – ostra białaczka szpikowa, SAA – ciężka postać anemii aplastycznej, CML – przewlekła białaczka szpikowa, HD – choroba Hodgkina, RMS – mięsak prążkowanokomórkowy, JMML – młodzieńcza białaczka mielomonocytowa, ES – mięsak Ewinga, NHL – chłoniak nieziarniczy, WAS – zespół Wiskott-Aldrich, MAC – kondycjonowanie mieloablacyjne, RIC – kondycjonowanie o zredukowanej toksyczności, TBI – frakcjonowane całkowite napromienianie ciała, CHT – chemioterapia, MFD – zgodny dawca rodzinny
W grupie pacjentów, u których zastosowano palifermin, wykazano niższe ryzyko wystąpienia ciężkiego OM (stopień 3-4 wg WHO), niż u pozostałych pacjentów (OR 5,5; p< 0,0001) (tab. 2). Pacjenci ci również rzadziej wymagali podawania morfiny w łagodzeniu objawów OM (OR 2,7; p = 0,05). Poza tym u pacjentów, u których zastosowano palifermin, istniało ponad 3,7-krotnie niższe ryzyko wystąpienia aGVHD niż w grupie bez paliferminu (p = 0,005), a także 3-krotnie niższe ryzyko wystąpienia cGVHD (p = 0,030). Stosowanie paliferminu nie wpłynęło istotnie na skrócenie czasu żywienia parenteralnego w obu analizowanych grupach (p = 0,060).
Tabela 2. Wpływ zastosowania paliferminu na wystąpienie ciężkiej postaci zapalenia śluzówek, użycie morfiny, wystąpienie n aGVHD ≥ 2 i cGVHD oraz czasu stosowania TPN.
aGVHD – ostra postać choroby przeszczep przeciwko gospodarzowi, cGVHD – przewlekła postać choroby przeszczep przeciwko gospodarzowi, TBI – frakcjonowane całkowite napromienianie ciała, OM – zapalenie śluzówek jamy ustnej, TPN – całkowite żywienie pozajelitowe, OR – iloraz szans, CI – przedział ufności, p – poziom istotności statystycznej
Spośród 79 pacjentów, u których stosowano palifermin, działania niepożądane leku obserwowano tylko w jednym przypadku. Polegały one na występowaniu uogólnionego rumienia skóry z towarzyszącym świądem całego ciała.
U pacjentów poddanych transplantacji od zgodnego dawcy rodzinnego (MFD-HSCT) istniało 4,5-krotnie większe ryzyko wystąpienia ciężkiego OM w grupie pacjentów bez paliferminu, niż u pacjentów z paliferminem (72,7 vs 37,0%; p = 0,012). Równocześnie u tych badanych w podgrupie bez paliferminu istniało znamiennie wyższe ryzyko wystąpienia cGVHD niż w podgrupie z paliferminem (36,4 vs 7,4%; p = 0,028). W podgrupie tej nie wykazano natomiast istotnych statystycznie różnic w ryzyku wystąpienia aGVHD, użyciu morfiny oraz czasu stosowania TPN.
Wśród pacjentów poddanych transplantacji od dawcy alternatywnego u pacjentów, którzy nie otrzymali paliferminu, stwierdzono znamiennie wyższe ryzyko wystąpienia ciężkiego OM (70,0 vs 28,8%; OR 5,9; p = 0,026) oraz konieczność stosowania morfiny (40,0 vs 13,5%; OR 5,1; p = 0,046). W podgrupie tej nie wykazano natomiast istotnych statystycznie różnic w ryzyku wystąpienia aGVHD, cGVHD oraz czasu stosowania TPN.
Wśród pacjentów, u których w kondycjonowaniu stosowano jedynie chemioterapię, stwierdzono niższe ryzyko wystąpienia OM u pacjentów, którzy otrzymali palifermin (26,7 vs 68%; OR 5,7; p = 0,0009). W podgrupie otrzymującej palifermin istniało również mniejsze ryzyko wystąpienia aGVHD (10 vs 32%; OR 4,2; p = 0,22), cGVHD (8,3 vs 28%; OR 4,3; p = 0,035), a także potrzeba krótszego żywienia parenteralnego (16 vs 21 dni; p = 0,042). W analizowanych podgrupach równie często konieczne było stosowanie morfiny.
U pacjentów, u których zastosowano kondycjonowanie oparte na radio- i chemioterapii nie obserwowano istotnych statystycznie różnic pomiędzy analizowanymi podgrupami (z paliferminem/bez paliferminu), wynikające najprawdopodobniej z małej ilości pacjentów w poszczególnych podgrupach.
Analiza czasu wolnego od choroby (pDFS) pośród wszystkich badanych pacjentów wykazała lepsze przeżycie u pacjentów, którzy otrzymywali palifermin, niż u tych, którzy paliferminu nie otrzymywali (0,67 ± 0,09 vs 0,509 ± 0,055; p = 0,019). Natomiast analiza całkowitego przeżycia (pOS) nie wykazała istotnych statystycznie różnic pomiędzy badanymi grupami (p = 0,29) (ryc. 1).
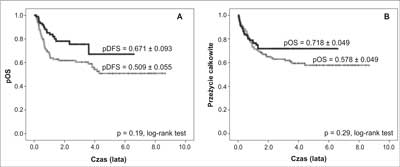 Ryc. 1 Wpływ paliferminu na (A) przeżycie wolnego od choroby (pDFS) oraz (B) przeżycie całkowite (pOS).
Dyskusja
Pomimo coraz większej ilości danych na temat zastosowania paliferminu u dorosłych poddawanych transplantacji komórek krwiotwórczych, dane na temat użycia tego leku u dzieci i młodzieży są ograniczone (3). Zagadnienie to jest tym bardziej istotne, że ryzyko wystąpienia OM jest prawdopodobnie większe u pacjentów pediatrycznych niż u dorosłych (3). W opinii pacjentów poddanych transplantacji komórek krwiotwórczych zapalenie śluzówek jamy ustnej jest jednym z najbardziej wyczerpujących powikłań podczas całej procedury transplantacji (2).
W opracowaniu Blazar i wsp. (9), w grupie pacjentów, u których zastosowano palifermin, obserwowano zmniejszenie częstości oraz stopnia nasilenia OM u tych, którzy byli kondycjonowani przy użyciu cyklofosfamidu w połączeniu z TBI, lecz nie przy użyciu busulfanu z cyklofosfamidem. Podobne wyniki obserwowali również Goldberg i wsp. (13). Natomiast w naszym opracowaniu obserwowano znamiennie rzadsze występowanie ciężkiego zapalenia śluzówek jamy ustnej, zarówno wśród wszystkich analizowanych pacjentów poddanych allogenicznej transplantacji komórek krwiotwórczych, jak i w poszczególnych analizowanych podgrupach. Obserwacja ta potwierdziła się również w podgrupie pacjentów, u których zastosowano chemioterapię w kondycjonowaniu (wśród 60 pacjentów otrzymujących palifermin 40 z nich miało kondycjonowanie oparte na busulfanie). Z kolei w grupie pacjentów, u których zastosowano łącznie TBI w kondycjonowaniu, nie obserwowano istotnego wpływu paliferminu. Możliwe że liczebność grupy pacjentów otrzymujących TBI w naszej analizie uniemożliwia wykazanie istotnych statystycznie różnic pomiędzy podgrupami.
Sposób kondycjonowania nie wpływał na konieczność użycia morfiny pośród badanych pacjentów. Obserwowano natomiast, że u pacjentów otrzymujących przeszczep od dawcy alternatywnego rzadziej istniała konieczność użycia morfiny w łagodzeniu objawów OM. Podobnie w badaniach innych autorów obserwowano zmniejszenie częstości użycia opioidów w łagodzeniu objawów OM (2, 14), a także lepszą kontrolę analgezji u pacjentów, którzy otrzymywali palifermin (13).
U pacjentów, u których zastosowano w kondycjonowaniu jedynie chemioterapię, otrzymujących palifermin, obserwowano znamiennie niższe ryzyko wystąpienia ciężkiej postaci ostrej choroby przeszczep przeciwko gospodarzowi (aGVHD ≥ 2 stopnia). W pozostałych analizowanych podgrupach takich zależności nie obserwowano. W analizach obejmujących pacjentów dorosłych nie obserwowano wpływu użycia paliferminu na rozległość i ryzyko występowania aGVHD (9, 13-15) i jedynie w pracy Nasilowskiej-Adamskiej i wsp. sugerowano związek pomiędzy stosowaniem paliferminu i mniejszym ryzykiem aGVHD (2).
U pacjentów poddanych transplantacji od zgodnego dawcy rodzinnego oraz pacjentów kondycjonowanych bez użycia TBI użycie paliferminu zmniejszało ryzyko wystąpienia aGVHD i cGVHD. Nasze obserwacje obejmujące grupę dzieci i młodzieży różnią się od obserwacji przeprowadzonych przez innych autorów wśród pacjentów dorosłych, u których nie obserwowano wpływu użycia paliferminu na częstość aGVHD i cGVHD (9, 13, 15).
U pacjentów dorosłych nie obserwowano wpływu użycia paliferminu na przeżycie całkowite w okresie potransplantacyjnym (9, 14, 15). Podobnie w naszym opracowaniu u dzieci i młodzieży nie obserwowano wpływu zastosowania paliferminu na prawdopodobieństwo całkowitego przeżycia pośród wszystkich analizowanych pacjentów poddanych transplantacji allogenicznych komórek krwiotwórczych.
Wśród wszystkich analizowanych pacjentów oraz w poszczególnych podgrupach nie obserwowaliśmy wpływu podania paliferminu na czas stosowania TPN. Jedynie u pacjentów, u których zastosowano jedynie chemioterapię w kondycjonowaniu, obserwowano, że palifermin skraca czas TPN. Natomiast w badaniu Goldberg i wsp. obserwowano krótszy okres TPN w grupie z paliferminem, która otrzymywała TBI w kondycjonowaniu (13). Natomiast w badaniu Johansson i wsp. obserwowano zmniejszenie konieczności stosowania TPN u pacjentów poddawanych autologicznej transplantacji komórek krwiotwórczych w oparciu o chemioterapię BEAM (16).
Palifermin był dobrze tolerowany przez dzieci i młodzież, a objawy niepożądane pod postacią uogólnionego rumienia ciała i świądu wystąpiły jedynie u 1 na 79 pacjentów, u których zastosowano palifermin. Podobnie w badaniu Johansson i wsp. nie obserwowano żadnych objawów niepożądanych działania paliferminu u wszystkich 17 badanych pacjentów (16). Również w obserwacji innych autorów palifermin był dobrze tolerowany przez pacjentów dorosłych, a najczęstszymi objawami niepożądanymi były: łagodne objawy pod postacią zaczerwienienia, świądu, rumienia, obrzęku, podwyższonej ciepłoty ciała, bólów stawów, dolegliwości ze strony języka lub jamy ustnej oraz zaburzenia czucia smaku (9, 14, 17, 18).
Wnioski
1. Palifermin jest bezpiecznym lekiem stosowanym u dzieci i młodzieży poddanych transplantacji allogenicznych komórek krwiotwórczych.
2. Zastosowanie tego leku u dzieci i młodzieży wiąże się z istotnym zmniejszeniem powikłań związanych z uszkodzeniem błon śluzowych oraz zmniejszeniem ryzyka rozwoju ostrej i przewlekłej choroby GVHD. Piśmiennictwo
1. Jahangard-Rafsanjani Z, Gholami K, Hadjibabaie M et al.: The efficacy of selenium in prevention of oral mucositis in patients undergoing hematopoietic SCT: A randomized clinical trial. Bone Marrow Transplant 2013; 48: 832-836.
2. Nasilowska-Adamska B, Rzepecki P, Manko J et al.: The influence of palifermin (kepivance) on oral mucositis and acute graft versus host disease in patients with hematological diseases undergoing hematopoietic stem cell transplant. Bone Marrow Transplant 2007; 40: 983-988.
3. Miller MM, Donald DV, Hagemann TM: Prevention and treatment of oral mucositis in children with cancer. J Pediatr Pharmacol Ther 2012; 17: 340-350.
4. Robien K, Schubert MM, Bruemmer B et al.: Predictors of oral mucositis in patients receiving hematopoietic cell transplants for chronic myelogenous leukemia. J Clin Oncol 2004; 22: 1268-1275.
5. Otmani N, Alami R, Hessissen L et al.: Determinants of severe oral mucositis in paediatric cancer patients: A prospective study. Int J Paediatr Dent 2011; 21: 210-216.
6. Papas AS, Clark RE, Martuscelli G et al.: A prospective, randomized trial for the prevention of mucositis in patients undergoing hematopoietic stem cell transplantation. Bone Marrow Transplant 2003; 31: 705-712.
7. Kennedy L, Diamond J: Assessment and management of chemotherapy-induced mucositis in children. J Pediatr Oncol Nurs 1997; 14: 164-174.
8. Vokurka S, Steinerova K, Karas M et al.: Characteristics and risk factors of oral mucositis after allogeneic stem cell transplantation with FLU/MEL conditioning regimen in context with BU/CY2. Bone Marrow Transplant 2009; 44: 601-605.
9. Blazar BR, Weisdorf DJ, Defor T et al.: Phase 1/2 randomized, placebo-control trial of palifermin to prevent graft-versus-host disease (GVHD) after allogeneic hematopoietic stem cell transplantation (HSCT). Blood 2006; 108: 3216-3222.
10. Miller AB, Hoogstraten B, Staquet M et al.: Reporting results of cancer treatment. Cancer 1981; 47: 207-214.
11. Przepiorka D, Weisdorf D, Martin P et al.: 1994 consensus conference on acute GVHD grading. Bone Marrow Transplant 1995; 15: 825-828.
12. Filipovich AH, Weisdorf D, Pavletic S et al.: National Institutes of Health consensus development project on criteria for clinical trials in chronic graft-versus-host disease. I. Diagnosis and staging working group report. Biol Blood Marrow Transplant 2005; 11: 945-956.
13. Goldberg JD, Zheng J, Castro-Malaspina H et al.: Palifermin is efficacious in recipients of TBI-based but not chemotherapy-based allogeneic hematopoietic stem cell transplants. Bone Marrow Transplant 2013; 48: 99-104.
14. Langner S, Staber P, Schub N et al.: Palifermin reduces incidence and severity of oral mucositis in allogeneic stem-cell transplant recipients. Bone Marrow Transplant 2008; 42: 275-279.
15. Nasilowska-Adamska B, Szydlo R, Rzepecki P et al.: Palifermin does not influence the incidence and severity of GVHD nor long-term survival of patients with hematological diseases undergoing hsct. Ann Transplant 2011; 16: 47-54.
16. Johansson JE, Hasseus B, Johansson P et al.: Gut protection by palifermin during autologous haematopoietic SCT. Bone Marrow Transplant 2009; 43: 807-811.
17. Fliedner M, Baguet B, Blankart J et al.: Palifermin for patients with haematological malignancies: Shifting nursing practice from symptom relief to prevention of oral mucositis. Eur J Oncol Nurs 2007; 11 (suppl. 1): 19-26.
18. Srinivasan A, Kasow KA, Cross S et al.: Phase I study of the tolerability and pharmacokinetics of palifermin in children undergoing allogeneic hematopoietic stem cell transplantation. Biol Blood Marrow Transplant 2012; 18: 1309-1314.
otrzymano/received: 2013-07-22 zaakceptowano/accepted: 2013-08-26 Adres/address: *Jan Styczyński Klinika Pediatrii, Hematologii i Onkologii Collegium Medicum UMK ul. Curie-Skłodowskiej 9, 85-094 Bydgoszcz tel.: +48 (52) 585-48-60, fax: +48 (52) 585-48-67 e-mail: jstyczynski@cm.umk.pl Artykuł Zastosowanie paliferminu u dzieci i młodzieży poddawanych transplantacji allogenicznych komórek krwiotwórczych w Czytelni Medycznej Borgis. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Chcesz być na bieżąco? Polub nas na Facebooku: strona Wydawnictwa na Facebooku |








