|
© Borgis - Postępy Nauk Medycznych 8, s. 628-635
*Tomasz Krosny, Paweł Dąbek, Walerian Staszkewicz, Adam Lewszuk
Ocena zaburzeń ukrwienia u pacjentów z miażdżycowym niedokrwieniem kończyn dolnych za pomocą analizy nirs (spektroskopia w bliskiej podczerwieni)
Assesment of perfusion abnormalities in patients with p.o.d. using NIRS (near infrared spectroscopy)
Klinika Chirurgii Naczyniowej i Angiologii Centrum Medycznego Kształcenia Podyplomowego, Szpital Bielański im. ks. Jerzego Popiełuszki
Kierownik Kliniki: prof. dr hab. med. Walerian Staszkiewicz Streszczenie
Przewlekłe niedokrwienie kończyn dolnych (PNKD) stanowi powszechny problem zdrowotny, u podłożu którego leży zmniejszenie przepływu krwi tętniczej w obrębie kończyn. Pomimo szybkiego rozwoju nowych technik operacyjnych, metody diagnostyczne w PNKD są w znacznym stopniu nieprecyzyjne w określaniu prawdziwej przyczyny choroby – zmniejszenia utlenowania niedokrwionych mięśni. W diagnostyce używanych jest obecnie wiele różnych metod, w tym: badanie tętna, wskaźnik kostkowo-ramienny, usg metodą dopplera, arteriografia, angiotomografia. Metody te pozwalają ocenić morfologię i przepływ w naczyniu tętniczym, nie można jednak za ich pomocą określić utlenowania zaopatrywanych tkanek, co jest podstawą prawidłowego funkcjonowania kończyny. Badania prężności tlenu (TcpO2) czy metodą laser Doppler, pozwalają ocenić przepływ w mikrokrążeniu tylko w powierzchownych warstwach tkanek (głównie w obrębie skóry). Technologia NIRS pozwala mierzyć zwartość utlenowanej hemoglobiny w tkankach. Obliczenia dokonywane na podstawie zmodyfikowanego prawa Beer-Lamberta pozwalają na podstawie różnicy w zawartości hemoglobiny wysyconej tlenem i zredukowanej określić zużycie tlenu w tkankach. Światło w zakresie fal podczerwieni jest emitowane przez optody i absorbowane przy przejściu przez tkanki w różnym stopniu, w zależności od ich utlenowania. NIRS jest używany od lat 80. XX wieku w różnych dziedzinach medycyny, mi.n. do oceny przepływu mózgowego w trakcie endarterektomii tętnic szyjnych; u pacjentów w oddziałach intensywnej terapii z niewydolnością oddechową; u wcześniaków; u pacjentów dializowanych; pacjentów z chromaniem przestankowym w diagnostyce PNKD. Metoda jest bezinwazyjna i nie wywołuje powikłań. NIRS w połączeniu z testem okluzyjnym jest metodą, za pomocą której można wywołać niedokrwienie kończyny, jakie występuje podczas chromania przestankowego. Cel pracy. Ocena badania za pomocą NIRS, jako narzędzia służącego do oceny skuteczności leczenia operacyjnego – rewaskularyzacji. Materiał i metody. Badaniem objęto 20 pacjentów z PNKD poddanych rewaskularyzacji operacyjnej. Badanie NIRS podczas testu okluzyjnego było przeprowadzane przed i we wczesnym okresie pooperacyjnym. Obserwowano różnice w zawartości w tkankach podudzia hemoglobiny utlenowanej (O2Hb) i zredukowanej (HHb), zmiany wskaźnika utlenowania tkanek (TOI), czasu reperfuzji (TR) oraz przekrwienia reaktywnego (PR). Wyniki. Zaobserwowano różnice w parametrach NIRS przed i po leczeniu operacyjnym. Większe wartości zmian parametrów O2Hb, Hhb i TOI zaobserwowano po rewaskularyzacji. Czas reperfuzji po operacji uległ skróceniu. Nie zaobserwowano istotnych zmian w zakresie przekrwienia reaktywnego. Wnioski. Badanie NIRS w połączeniu z testem okluzyjnym pozwala na wczesną ocenę rezultatów leczenia operacyjnego w zakresie poprawy utlenowania niedokrwionych tkanek. Słowa kluczowe: spektroskopia bliskiej podczerwieni, przewlekłe niedokrwienie kończyn dolnych, tkankowe zużycie tlenu, chromanie przestankowe, chirurgia naczyniowa
Summary
Peripheral arterial dissease (PAD) is a common health problem caused by reduced blood flow to the limbs. Alltough rapid development of surgery in recent years gives a modern surgical techniques, the diagnostic methods are still beeing imprecise in detecting nature of dissease – the reduction of oxygen consumption rate in skeletal muscle. Several techniques are curently beeing used to aid the diagnosis and severity assessment of patients with PAD. These include ankle-bracial index (ABI), pulse palpation, dupplex ultrasound, arteriography, computed tomography – asses blood suply but not oxygen and nutrient transport essential for limb functionality. TcpO2 and laser Doppler are used to asses blood flow fiirst of all in the surface of skin. Near infrared spectroscopy (NIRS) is a technology in which oxygen saturation of haemoglobin is measured using near infrared light. By the applying of modyfied Beer-Lambert law is possible to calculate the saturation of haemoglobin in examinated tissues. The light is emitted through muscle tissue, absorbed to a different degree, depending on the relative concentrations of oxy- and deoxyhaemoglobin. NIRS has been used since the eightees for the assesment of cerebral circulation during carotid endarterectomy in critically ill patients with sepsis, in dialised patients, in patients with claudications. This method is easily applicable and non-invasive. NIRS combined with the vascular occlusion technique is a promising approach for the evaluation of the standard duration ischaemic stimulus in patients with PAD and claudication. Aim. The aim of this study is the assesment of NIRS as a method for the evaluation of operative revascularistion. Material and methods. 20 patients with PAD were studied. The occlusion test with NIRS was performed before and after the oparation. Variations in oxygenated haemoglobin (Hbo2), deoxygenated haemoglobin (Hhb), tissue oxygenation index (TOI), time of recovery and reactive hyperaemia was recorded. Results. The differences was observed in patients after and before operation. Major changes in O2Hb and Hhb and TOI were observed in patients after operation. Time of recovery was shortened in patients after operation. There were no differences in patients in reactive hyperaemia in early postoperative period. Conclusions. The occlusion NIRS test allows the evaluation of early posoperative results in patients with PAD. Key words: near infrared spectroscopy, peripheral arterial dissease, intermittent claudication, oxygen consumption rate, vascular surgery
Przewlekłe niedokrwienie kończyn dolnych (PNKD, ang. PAD – peripheral arterial dissease) dotyczy wg badań epidemiologicznych 3-10% populacji, wzrastając do 15-20% u osób powyżej 70. roku życia (1). Klasycznym objawem przewlekłego niedokrwienia kończyn dolnych jest wystąpienie chromania przestankowego, istnieje jednak duża grupa osób, u których choroba przebiega bezobjawowo (wg różnych autorów stosunek pomiędzy obiema grupami wynosi 1:3 do 1:4) (1). Wyniki epidemiologiczne z ostatnich 40 lat pokazały, że tylko u 25% pacjentów z chromaniem nastąpi znacząca progresja choroby, a u ok. 3% wystąpi krytyczne niedokrwienie kończyny dolnej a więc stan, w którym kończyna zagrożona jest amputacją (1, 2).
Niemniej jednak pacjenci z PAD stanowią przeważający odsetek chorych poddawanych leczeniu operacyjnemu w oddziałach chirurgii naczyniowej.
U podstaw patofizjologii przewlekłego miażdżycowego niedokrwienia kończyn dolnych leży niedotlenienie tkanek. Zwężenia tętnic powodują zmniejszony dopływ krwi, zawierającej utlenowaną hemoglobinę, do tkanek leżących dystalnie od zwężenia. Powoduje to zaburzenia metaboliczne, które odpowiedzialne są za wystąpienie dolegliwości, a z czasem do powstania głębokiego niedokrwienia i martwicy tkanek.
Celem operacji, którym poddawani są chorzy z PAD jest rewaskularyzacja, czyli przywrócenie dostatecznego krążenia krwi tętniczej, zawierajacej utlenowaną hemoglobinę do tkanek leżących obwodowo od zwężonego lub niedrożnego odcinka naczynia. Efektem, który chirurg powinien uzyskać jest poprawienie utlenowania tych tkanek, co jest niezbędne dla ich prawidłowego funkcjonowania.
W chwili obecnej chirurgia naczyniowa dysponuje coraz bardziej zróżnicowanymi i zaawansowanymi metodami operacyjnymi, wśród których coraz większą rolę pełnią zabiegi endowaskularne. Bez względu na rodzaj zastosowanej metody operacyjnej cel pozostaje jednak ten sam – poprawa dostarczenia przez krew tlenu do niedokrwionych tkanek.
Coraz szybszemu rozwojowi metod operacyjnych nie towarzyszy jednak zwiększenie możliwości rzeczywistej, obiektywnej oceny skuteczności zabiegu w bezpośrednim okresie pooperacyjnym. Metody, którymi dysponujemy niosą ze sobą liczne ograniczenia. Stwierdzany po operacji wzrost ciepłoty kończyny, ustąpienie bólów spoczynkowych, pojawienie się tętna na tętnicach obwodowych, czy wzrost wartości wskaźnika ABI (ankle-brachial index, wskaźnik kostkowo-ramienny) pozwalają ocenić przepływ krwi w dużych, poddanych operacji naczyniach. Podobnie badanie usg dopplerowskie czy komputerowa angiografia. W bezpośrednim okresie pooperacyjnym wykonanie testu wysiłkowego, który pozwoliłby na ocenę dystansu chromania przestankowego jest jeszcze niemożliwe. Przepływ w ocenianych w ten sposób tętnicach, jakkolwiek jest widocznym wskaźnikiem pomyślności technicznego przeprowadzenia zabiegu, nie jest jednoznaczny z poprawą przepływu w mikrokrążeniu, w którym dochodzi do rzeczywistej wymiany gazowej. Metody stosowane w celu oceny mikrokrążenia (np. laser doppler, Tcpo2) mają również swoje ograniczenia – odzwierciedlają stan mikrokrążenia w powierzchownych warstwach tkanek, podczas gdy objawy PAD związane są głównie z niedotlenieniem głębiej położonych grup mięśniowych (3).
Wydaje się istotne znalezienie metody diagnostycznej, pozwalającej na rzeczywistą ocenę poprawy utlenowania tkanek, a więc podstawowego celu, który przyświeca zabiegom rewaskularyzacyjnym. Metody, która w obiektywny sposób pozwoli ocenić nie tylko zwiększenie napływu krwi, ale również podstawową funkcję krążenia – poprawę metabolizmu tkanek, który prawidłowo przebiega jedynie przy udziale tlenu, a do którego konieczne jest prawidłowe funkcjonowanie również naczyń mikrokrążenia.
Wydaje się, że metodą taką może być analiza wykonana za pomocą spektroskopii bliskiej podczerwieni (NIRS – near infrared spectroscopy). Od czasu pierwszego opisania tej metody w roku 1977 (Jobsis) jest ona wykorzystywana, chociaż niezbyt rozpowszechniona, w różnych dziedzinach medycyny (4, 5). Znalazła już ona zastosowanie w diagnostyce pacjentów z PAD (5-9), u chorych z niewydolnością oddechową i sepsą leczonych w oddziałach intensywnej terapii (10-12), chorych poddawanych hemodializie (13), chorych z niewydolnością serca (14-16). Wykazano również jej skuteczność podczas badania wpływu palenia papierosów na utlenowanie tkanek (16). W piśmiennictwie pojawiły się nieliczne prace, w których zastosowano NIRS w sposób ciągły monitorując przebieg operacji tętnic kończyn dolnych (17).
Ważne i praktyczne zastosowanie znajduje również podczas operacji zwężenia tętnic szyjnych, w celu oceny wydolności krążenia mózgowego (18, 19).
Liczne dotychczas przeprowadzone badania udowodniły, że za pomocą analizy NIRS można w bezpieczny, bezinwazyjny sposób ocenić stopień i zmiany wysycenia tkanek organizmu tlenem.
Przegląd literatury zawiera prace przedstawiane przez różnych autorów, ukierunkowane na ocenę NIRS jako narzędzia diagnostycznego w PAD. Porównanie grupy kontrolnej osób zdrowych i chorych z PAD wykazało znamienne statystycznie różnice pomiędzy tymi grupami, głównie w zakresie takich parametrów, jak czas reperfuzji i przekrwienie reaktywne. Autorzy zgodni są do tego, że konieczne jest zastosowanie testów wysiłkowych lub testu okluzyjnego aby wykazać ww. różnice (20, 21). Próby porównywania grupy kontrolnej z chorymi na PAD w spoczynku nie wykazywały pomiędzy nimi uchwytnych różnic w badaniu NIRS (6, 7, 22, 23). Wyniki uzyskane przy pomocy analizy NIRS wykazywały korelację z innymi metodami diagnostycznymi (ABI, usg) (7, 23, 24). Wykazano również, że NIRS może być także w pewnym stopniu wykorzystane w celu oceny stopnia zaawansowania zmian miażdżycowych (25).
Potwierdzono doświadczalnie powtarzalność badań przy użyciu NIRS (7, 20). Zwraca się również uwagę, że NIRS jest metodą prostą technicznie, o krótkiej krzywej uczenia, oraz nie generuje działań ubocznych – jest więc to metoda bezpieczna (3).
Wychodząc z założenia, że istotą PAD jest niedokrwienie tkanek prowadzące do ich niedotlenienia, założono że skuteczna rewaskularyzacja operacyjna powinna znajdować odzwierciedlenie na poziomie nie tylko naczyń, ale przede wszystkim tkanek, a zmiany parametrów ocenianych w NIRS powinny być obiektywnym ich wyznacznikiem. Za pomocą NIRS możnaby więc w sposób obiektywny ocenić skuteczność operacji, być może również z dużym prawdopodobieństwem przewidzieć dalszy przebieg choroby.
W Klinice Chirurgii Naczyniowej i Angiologii CMKP metoda NIRS jest od ok. 10 lat używana jako metoda dodatkowa oceny krążenia mózgowego podczas operacji endarterektomii tętnic szyjnych. Zmiany w obserwowanych zapisach, obrazujących przepływ mózgowy korelują z momentem zacisku klemu na tętnicach szyjnych i przywróceniu krążenia mózgowego. Analiza przebiegu krzywej pozwala również ocenić wydolność koła tętniczego mózgu. Obecnie zaplanowano protokół badania mającego przy pomocy badania NIRS określić skuteczność operacyjnej rewaskularyzacji u chorych z przewlekłym niedokrwieniem kończyn dolnych.
CEL Pracy
Zasadniczym celem pracy jest:
1. Znalezienie odpowiedzi na pytanie, czy zastosowanie spektroskopii w bliskiej podczerwieni może być metodą, pozwalającą na obiektywną ocenę i parametryzację poprawy ukrwienia kończyn dolnych po leczeniu operacyjnym u chorych z przewlekłym niedokrwieniem kończyn dolnych.
2. Próba odpowiedzi na pytanie, czy NIRS może mieć zastosowanie jako metoda prognostyczna, pomocna w planowaniu dalszego leczenia.
MATERIAŁ I METODY
Do badania włączono grupę chorych z przewlekłym miażdżycowym niedokrwieniem kończyn dolnych, u których zaplanowano leczenie operacyjne (metodą endowaskularną lub tradycyjną). Podstawą kwalifikacji była obecność zmian miażdżycowych w obrębie tętnic biodrowych i/lub udowych.
Grupę badaną stanowiło 20 pacjentów. Wszyscy zaliczali się do grupy II wg klasyfikacji Fontaine‘a. Sposób badania został zaaprobowany przez komisję bioetyczną CMKP. Pacjenci zostali poinformowani o sposobie przeprowadzenia, celu badania oraz możliwych powikłaniach i podpisali formularz świadomej zgody. Wszyscy byli badani w godzinach przedpołudniowych, w tym samym pomieszczeniu o temperaturze powietrza 21°C. Charakterystyka kliniczna grupy została przedstawiona w tabeli 1. Od każdego chorego zebrano wywiad chorobowy, wykonano standardowe badanie przedmiotowe i określono wskaźnik kostkowo-ramienny (K/R, ABI) wg zaleceń zawartych w TASC II.
Tabela 1. Charakterystyka grupy badanej. Badanie przedoperacyjne.
Zaplanowano protokół badania obejmujący pomiary za pomocą aparatu NIRO, po wykonaniu standardowego testu okluzyjnego. Test ten przeprowadzano za pomocą mankietu do pomiaru ciśnienia tętniczego krwi. Mankiet ciśnieniomierza zakładany był bezpośrednio poniżej kolana, następnie na okres 5 minut napompowany do ciśnienia o 50 mm Hg wyższego niż wyższe z ciśnień skurczowych mierzonych na obu ramionach, jednocześnie rejestrowano zanik przepływu na tętnicach stopy za pomocą UDP (ultradźwiękowy detektor przepływu). Badany przez cały okres pozostawał w pozycji leżącej. Optody mocowane były każdorazowo na tylnej powierzchni podudzia, poniżej mankietu, w uchwycie gwarantującym zachowanie tej samej odległości między optodą emisyjną i detekcyjną. Odległość ta wynosiła 4 cm u wszystkich badanych. Obszar poddany badaniu mieści się między 2 a 6 cm3. Badania wykonywane były przy użyciu urządzenia NIRO-200 firmy HAMAMATSU wykorzystującego nieinwazyjną technikę pomiaru w bliskiej podczerwieni. Urządzenie to korzysta ze światła o długości fali 700-950 nm przechodzącego dość dobrze przez tkanki ludzkie i częściowo pochłanianego przez nośniki tlenu jak hemoglobina, mioglobina i cytochrom aa3. Obliczenia dokonywane są automatycznie według zmodyfikowanego prawa Beer-Lamberta (które opisuje pochłanianie promieniowania elektromagnetycznego przy przechodzeniu przez częściowo absorbujący i rozpraszający ośrodek) i metody spektroskopii przestrzennej. Głównym powodem zmiany absorpcji światła podczerwieni są zmiany w utlenowaniu i koncentracji hemoglobiny. Zmiany w utlenowaniu hemoglobiny są odbiciem różnicy pomiędzy ilością tlenu dostarczanego a wykorzystanego. Na tej podstawie możemy wnioskować o wydolności naczyń mikrokrążenia odpowiedzialnych za prawidłowy transport tlenu dostarczonego przez krew do tkanek. Ocena bezwzględnych wartości hemoglobiny utlenowanej, zredukowanej bądź całkowitej metodą NIRS jest trudna, nie można też ustanowić norm obowiązujacych powszechnie. Aby to osiągnąć niezbędna jest znajomość tzw. optycznej długości ścieżki światła L (cm), która jest wartością specyficzną dla badanych tkanek, trudną do zmierzenia w warunkach in vivo, ale stałą dla badanego pacjenta. W tej sytuacji, aby w sposób porównywalny i czytelny przedstawić otrzymane wyniki, oceniana jest zmiana poziomu koncentracji hemoglobiny całkowitej (?CHb), utlenowanej (?O2Hb) i zredukowanej (?HHb), względem poziomu wyjściowego (21).
Analizie poddawane są poniżej przedstawione parametry:
– TOI (Tissue Oxygenation Index) – wskaźnik utlenowania tkanek, czyli stosunek (%) hemoglobiny utlenowanej do całkowitej,
– ?O2Hb, czyli zmiana poziomu utlenowanej hemoglobiny mierzona w μmol/l,
– ?HHb, czyli zmiana poziomu zredukowanej hemoglobiny mierzona w μmol/l,
Każdy z nich monitoruje się podczas próby w sposób ciągły.
Na podstawie wygenerowanego przez komputer wykresu dokonywano niezbędnych obliczeń. Schemat wykresu i najważniejsze zmienne przedstawiono poniżej (na podstawie krzywej ?O2Hb) (ryc. 1).
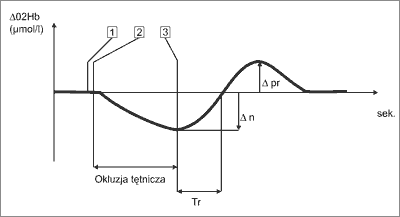 Ryc. 1. Schemat wykresu badania NIRS.
TR time of recovery – czas reperfuzji Δn – stopień niedokrwienia, czyli minimalna siła sygnału policzona względem stanu wyjściowego, mierzona w μmol/l O2Hb lub w procentach w przypadku pomiaru TOI Δpr – przekrwienie reaktywne (odczynowe), czyli maksymalna różnica siły sygnału pomniejszona o wartość wyjściową, mierzona w μmol/l O2Hb i HHB lub procentach w przypadku pomiaru TOI (wartości podawane w μmol/l O2Hb, μmol/l HHb lub w procentach w przypadku pomiaru TOI) 1 – początek pompowania mankietu sfingomanometru 2 – koniec pompowania mankietu, początek okluzji tętniczej 3 – gwałtowne wypuszczenie powietrza z mankietu (Δn) stopień niedokrwienia minimalna siła sygnału, liczona względem stanu wyjściowego
TR czas reperfuzji (time of recovery, reperfusion rate) czas powrotu krzywej do wartości wyjściowych, liczony od momentu spuszczenia powietrza z mankietu do momentu powrotu poziomu utlenowania do wartości wyjściowej. Parametr ten niezależnie wyliczano z trzech mierzonych wartości TOI, ?O2Hb, ?HHb. Długość Tr odzwierciedla mechanizm zależny w głównej mierze od integralności i prawidłowej funkcji śródbłonka naczyniowego.
Δpr przekrwienie reaktywne (reactive hyparaemia, vascular reserve) jest to maksymalna wartość sygnału NIRS pomniejszona o wartość spoczynkową; podczas niedokrwienia kończyny w fazie zaciśnięcia mankietu, hipoksja powoduje rozszerzenie naczyń mikrokrążenia, które po spuszczeniu mankietu prowadzi do reaktywnego przekrwienia. Stopień przekrwienia reaktywnego zależy wprost proporcjonalnie od zdolności mikrokrążenia do adekwatnej odpowiedzi na bodziec niedokrwienny.
Pierwszy pomiar odbywał się w przeddzień operacji, po przybyciu chorego do oddziału Chirurgii Naczyniowej.
Drugiego pomiaru dokonywano w trzeciej dobie po operacji metodą klasyczną (w drugiej dobie po operacji metodą endowaskularną).
Po wykonaniu badań nr 1 i nr 2 porównywano otrzymane wyniki.
Wizytę kontrolną (nr 3) zaplanowano po 30 dniach po operacji, kolejną (nr 4) w 90 dni po operacji. Podczas wizyt nr 3 i 4 nie planowano wykonywania pomiarów przy użyciu NIRS. Przeprowadzano wywiad i rutynowe badanie naczyniowe.
WYNIKI
U każdego pacjenta uzyskano wyniki w formie wykresu NIRS. Analizując wykres określano wartość spoczynkową, minimalną (po zastosowaniu okluzji) i maksymalną:
O2Hb, HHb oraz TOI.
Δn – stopień niedokrwienia (obliczono jako różnicę pomiędzy wartością spoczynkową danego parametru a wartością minimalną dla O2Hb I TOI, maksymalną dla HHb).
TR – Czas reperfuzji odczytwywano z wykresu jako czas pomiędzy zakończeniem okluzji a powrotem parametru do wartości spoczynkowej.
Δpr – przekrwienie reaktywne określono jako różnicę pomiędzy maksymalną wartością danego parametru (o2Hb I TOI) po ustaniu okluzji a wartością spoczynkową.
Po napompowaniu mankietu sfingomanometru obserwowano stopniowy spadek wartości utlenowanej hemoglobiny O2HB i wskaźnika utlenowania tkanek TOI oraz wzrost wartości zredukowanej hemoglobiny Hhb.
Po spuszczeniu powietrza z mankietu następował wzrost O2Hb i TOI oraz spadek Hhb. Tendencja ta utrzymywała się w badaniu nr 1 i nr 2.
W badaniu nr 1 (przed leczeniem operacyjnym) u wszystkich pacjentów po napompowaniu sfingomanometru wystapił: spadek wartości O2Hb wzrost wartości Hhb, spadek wartości TOI. Oceniano również wartości Δpr. Wyniki przedstawiono w tabeli 2.
Tabela 2. Badanie nr 1 – przed leczeniem operacyjnym.
W badaniu nr 2 (po rewaskularyzacji operacyjnej) również u wszystkich pacjentów po napompowaniu sfingomanometru stwierdzono: spadek wartości O2Hb, wzrost wartości Hhb, spadek wartosci TOI (wartości były wyższe niż w badaniu nr 1).
Po ustaniu okluzji czas reperfuzji uległ skróceniu w porównaniu do badania nr 1.
Wartości przekrwienia reaktywnego (Δpr), obliczonego na podstawie wykresów dla O2Hb i TOI nie różniły się w sposób istotny. Wyniki przedstawiono w tabeli 3.
Tabela 3. Badanie nr 2 – wczesne wyniki po przeprowadzonym leczeniu operacyjnym.
Następnie porównano otrzymane wyniki, co przedstawiono również w formie tabeli 4.
Tabela 4. Porównanie wyników pomiaru przed i po leczeniu operacyjnym.
Poniżej przedstawiono przykładowe wykresy otrzymane podczas badania przed operacją (ryc. 2) i po operacji (ryc. 3).
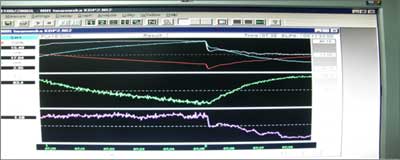 Ryc. 2. Badanie NIRS. Wykres otrzymany przed operacją (materiały własne autora).
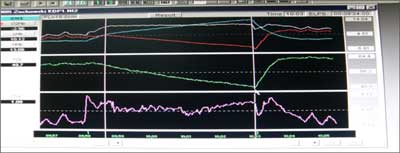 Ryc. 3. Badanie NIRS. Wykres otrzymany po operacji (materiały własne autora).
OMÓWIENIE WYNIKÓW. DYSKUSJA
Powtarzalność pomiarów metodą NIRS potwierdzono w licznych badaniach, przy czym pomiary na podudziu miały zdecydowanie lepszą korelacje niż pomiary wykonywane za pomocą optody mocowanej na grzbiecie stopy (10, 23).
W niniejszym badaniu nie poddawano ocenie i porównaniu różnych metod operacyjnych. Starano się wykazać, że dobry efekt operacji – skuteczna rewaskularyzacja obwodowa – powinien mieć odzwierciedlenie w poprawie perfuzji tkanek i funkcji mikrokrążenia.
Stopień niedokrwienia tkanek (Δn) obwodowych mierzony po operacji zwiększył się u wszystkich badanych pacjentów. Różnica pomiędzy wyjściowym poziomem O2Hb w tkankach a poziomem minimalnym w kończynie o lepszym ukrwieniu jest większa. Przed operacją zawartość utlenowanej Hb w tkankach jest niższa. Okluzja powoduje więc mniej nasilone objawy niedokrwienia. W tkankach o wyższej zawartości O2Hb, a więc u chorych po udanej rewaskularyzacji zastosowanie okluzji w większym stopniu nasila różnicę w wysyceniu utlenowaną hemoglobiną. Podobną prawidłowość zanotowano dla pomiarów zredukowanej Hb (Hhb).
Czas reperfuzji Tr ulega wydłużeniu u chorych z PAD, sepsą, niewydolnością serca, co zostało potwierdzone w badaniach (5, 14, 15, 29). Po skutecznej rewaskularyzacji TR uległ skróceniu średnio o 48 sek., tj o 71,75%. Stanowi to potwierdzenie uzyskanych w innych badaniach wyników, ukazujących dłuższy Tr w kończynie niedokrwionej. Czas reperfuzji jest związany z prawidłową funkcją śródbłonka i jednostki mikrokrążenia, która w kończynie niedokrwionej jest zaburzona. Poprawa utlenowania tkanek obwodowych po operacji związana jest ze skróceniem czasu reperfuzji, co jest również wyrazem poprawy funkcji mikrokrążenia.
Przekrwienie reaktywne Δpr zależy, jak wspomniano, od zdolności mikrokrążenia do adekwatnej odpowiedzi na bodziec, który stanowi hipoksja. W tkankach niedokrwionych odpowiedź ta jest słabsza. Parametr ten ulega zmniejszeniu w chorobach, w których dochodzi do niedotlenienia tkanek (5, 14, 17, 19). W przeprowadzonym badaniu przekrwienie reaktywne w tkankach po rewaskularyzacji było większe u 7 pacjentów, podczas gdy u 8 (czterech spośród nich chorowało na cukrzycę) było podobne lub niższe niż przed operacją. Być może wynika to z przeprowadzenia badania w niedługim okresie po operacji i na pełną poprawę właściwości mikrokrążenia potrzeba więcej czasu. Będzie to przedmiotem analizy w kolejnych badaniach po 30 dniach po operacji i dalszych.
Po leczeniu operacyjnym (rewaskularyzacja) potwierdzono poprawę utlenowania tkanek, będącą efektem przywrócenia przepływu krwi. Jak wspomniano w badaniu NIRS nie można określić wartości bezwzględnych badanych parametrów. Nie istnieją też określone normy, do których można odnosić uzyskane wyniki w wartościach bezwzględnych. W związku z tym analizę wyników przeprowadzono porównując charakter otrzymanych krzywych. Charakter zmian lepiej oddaje wyrażenie otrzymanych wyników w %, co lepiej oddaje rzeczywistą dynamikę i pozwala na zobrazowanie otrzymanych wyników. Odnosząc się do wyników uzyskanych przez autorów, badających zastosowanie NIRS w diagnostyce PAD, wnioskować możemy, że poprawie utlenowania tkanek odpowiada wzrost wartości Δ n i skrócenie TR (czasu reperfuzji). Prognozowany wzrost wartości Δpr nie znalazł potwierdzenia w badaniu bezpośrednio po operacji.
Według piśmiennictwa niektóre czynniki mogą wpływać na zburzenia pomiaru metodą NIRS. Niektóre publikacje wskazują, że w badaniu NIRS wyniki chorych z cukrzycą i zdrowych mogą nie wykazywać istotnych różnic. Autorzy wskazują, że u tych chorych zmiany w mikrokrążeniu powodujące uszkodzenie śródbłonka naczyniowego są odpowiedzialne za zaburzenia wazodilatacji i powodować mogą zafałszowanie wyników. W przedstawianym badaniu u 4 z 6 chorych na cukrzycę stwierdzono takie same lub mniejsze niż przed operacją przekrwienie reaktywne. Diagnostyka chorych z PAD i cukrzycą za pomocą NIRS może nie być metodą w pełni obiektywną, co jest przedmiotem dalszych badań (26, 30).
Na niedokładność pomiaru może mieć również wpływ nadmierna grubość tkanki tłuszczowej, co spowodwane jest zmniejszoną absorpcją światła przez tłuszcz (31). Podobny wpływ może wywierać również obrzęk kończyn dolnych (32). Niektórzy autorzy wspominają, że różnice może też powodować różny rozkład tkanki tłuszczowej związany z płcią (10, 19, 31).
Niewielkie ruchy kończyną podczas badania nie wpływają na zapis mierzonych parametrów.
WNIOSKI
1. Technika pomiaru NIRS jest badaniem łatwym do przeprowadzenia, bezpiecznym dla pacjenta.
2. Jest badaniem użytecznym i może stanowić uzupełnienie dotychczas stosowanych metod diagnostycznych, służących ocenie niedokrwienia kończyn dolnych również bezpośrednio po badaniu operacyjnym i może ułatwiać obiektywną ocenę skuteczności leczenia operacyjnego.
3. Ocena NIRS jako metody prognostycznej – w toku badania.
4. Badanie nie zostało jeszcze zakończone. Obecnie grupa badana jest rozszerzana w celu uzyskania danych umożliwiających wiarygodną ocenę statystyczną. Otrzymane wyniki wstępne wydają się potwierdzać przyjęte założenia i skłaniają do kontynuacji badań. Piśmiennictwo
1. TASC II. Inter Society Consensus for the Management of Peripheral Arterial Dissease. Eur J Vasc Endovasc Surg 2007; 33: S3-S68.
2. McDermott MM, Criqui MH, Greenland P et al.: Leg strength in peripheral arterial disease: associations with disease severity and lower-extremity performance. J Vasc Surg 2004; 39 (3): 523-530.
3. Fowkes FG, Housley E, Cawood EH et al.: Edinburgh Artery Study: prevalence of asymptomatic and symptomatic peripheral arterial dissease in the general population. Int J Epidemiol 1991; 20(2): 384-392.
4. Selvin E, Marinopoulos S, Berkenblit G et al.: Meta-analysis: glycosylated hemoglobin and cardiovascular disease in diabetes mellitus. Ann Intern Med 2004; 141(6): 421-31.
5. Raciborski W, Hendiger W, Staszkiewicz W: Spektroskopia w bliskiej podczerwieni i przepływy laserowo-dopplerowskie w ocenie ukrwienia kończyny dolnej po chemicznej sympatektomii lędźwiowej. Acta Angiologica 2002; 8: s. 25.
6. Vardi M, Nini A: Near-infrared Spectroscopy for Evaluation of Peripheral Vascular Disease. A Systematic Review of Literature. Eur J Vasc Endovasc Surg 2008; 35: 68-74.
7. Jobsis FF: Noninvasive, infrared monitoring of cerebral and myocardial oxygen sufficiency and circulatory parameters. Science 1977; 198: 1264-1267.
8. Cheatle TR, Potter LA, Cope M et al.: Near-infrared spectroscopy in peripheral vascular disease. Br J Surg 1991; 78 (4): 405-408.
9. Kooijman HM, Hopman MT, Colier WN et al.: Near infrared spectroscopy for noninvasive assessment of claudication. J Surg Res 1997; 72 (1): 1-7.
10. Ubbink DT, Koopman B: Near-infrared spectroscopy in the routine diagnostic work-up of patients with leg ischaemia. Eur J Vasc Endovasc Surg 2006; 31(4): 394-400.
11. Manfredini F, Malagoni AM, Felisatti M et al.: A dynamic objective evaluation of peripheral arterial disease by near-infrared spectroscopy. Eur J Vasc Endovasc Surg 2009; 38: 441-448.
12. De Blasi RA, Cope M, Elwell C et al.: Noninvasive measurement of human forearm oxygen consumption by near infrared spectroscopy. Eur J Appl Physiol Occup Physiol 1993; 67 (1): 20-25.
13. Pareznik R, Knezevic R, Voga G, Podbregar M: Changes in muscle tissue oxygenation during stagnant ischemia in septic patients. Intensive Care Med 2006; 32: 87-92.
14. Skarda DE, Mulier KE, Myers DE et al.: Dynamic nearinfrared spectroscopy measurements in patients with severe sepsis. Shock 2007; 27,348-353.
15. Creteur J, Carollo T, Soldati G et al.: The prognostic value of muscle StO2 in septic patients. Intensive Care Med 2007; 33: 1549-1556.
16. Kuge N, Suzuki T, Isoyama S: Does handgrip exercise training increase forearm ischemic vasodilator responses in patients receiving hemodialysis? Tohoku J Exp Med 2005; 207 (4): 303-312.
17. Nanas S, Gerovasili V, Dimopoulos S et al.: Inotropic agents improve the peripheral microcirculation of patients with end-stage chronic heart failure. J Card Fail 2008; 14 (5): 400-406.
18. Schachner T, Bonaros N, Bonatti J, Kolbitsch Ch: Near infrared spectroscopy for controlling the quality of distal leg perfusion in remote access cardiopulmonary bypass. Eur J Cardio-Thoracic S 2008; 34: 1253-1254.
19. Siafaka A, Angelopoulos E, Kritikos K et al.: Acute effects of smoking on skeletal muscle microcirculation monitored by near infrared spectroscopy. Chest 2007; 131: 1479-1485.
20. Eiberg JP, Schroeder TV, Vogt KC, Sechert NH: Near infrared spestroscopy during peripheral vascular surgery. Cardiovasc Surg 1997; 5, 3: 304-308.
21. Pennekamp CWA, Bots ML, Kapelle LJ et al.: The value of near-infrared spectroscopy measured cerebral oximetry during carotid endarterectomy in perioperative stroke prevention. A review. Eur J Vasc Endovasc Surg 2009; 38: 539-545.
22. Moritz S, Kasprzak P, Arlt M et al.: Accuracy of cerebral monitoring in detecting cerebral ischemia during carotid endarterectomy: a comparison of transcranial Doppler sonography, near-infrared spectroscopy,stump pressure, and somatosensory evoked potentials. Anesthesiology 2007; 107 (4): 563-569.
23. Mc Cully KK, Landsberg L, Suarez M et al.: Identification of peripheral vascular disease in elderly subjects using optical spectroscopy. J Gerontol A Biol Sci Med Sci 1997; 52(3): 159-165.
24. Harrison DK, Voss C, Vollmar HS et al.: Response of muscle oxygen saturation to exercise, measured with near infrared spectrophotometry in patients with peripheral vascular disease. Adv Exp Med Biol 1998; 454: 45-52.
25. Lee BY, Ostrander LE, Karmakar M et al.: Noninvasive quantification of muscle oxygen in subjects with and without claudication. J Rehabil Res Dev 1997; 34(1): 44-51.
26. Kragelj R, Jarm T, Erjavec T et al.: Parameters of postoclusive reactive hyperemia measured by near infrared spectroscopy in patients with peripheral vascular disease and in healthy volunteers. Ann Biomed Eng 2001; 29(4): 311-320.
27. Wolf U, Wolf M, Choi JH et al.: Localized irregularities in hemoglobin flow and oxygenation in calf muscle in patients with peripheral vascular disease detected with near infrared spectrophotometry. J Vasc Surg 2003; 37(5): 1017-1026.
28. Komiyama T, Shigematsu H, Yasahura H, Muto T: An objective assessment of intermittent claudication by near infrared spectroscopy. Eur J Vasc Surg 1994; 8(3): 294-296
29. Doerschug KC, Delsing AS, Scmidt GA, Haynes W: GImpairments in microvascular reactivity are related to organ failure in human sepsis. Am J Physiol. Heart Circ Physiol 2007; 293(2): H1065-H1071.
30. Mohler III ER, Lech G, Supple GE et al.: Impaired exercise-induced blood volume in type 2 diabetes with or without peripheral arterial disease measured by continuous-wave near infrared spectroscopy. Diabetes Care 2006; 29(8): 1856-1859.
31. Van Beekvelt MC, Borghuis MS, van Engelen BG et al.: Adipose tissue thickness affects in vivo quantitative near-IR spectroscopy in human skeletal muscle. Clin Sci (Lond) 2001; 101(1): 21-28.
32. Poeze M: Tissue oxygenation assessment using near infrared spectroscopy during severe sepsis: confounding effects of tissue edema on StO2 values. Intensive Care Med 2006; 32(5):788-789.
otrzymano/received: 2012-05-14 zaakceptowano/accepted: 2012-06-11 Adres/address: *Tomasz Krosny Klinika Chirurgii Naczyniowej i Angiologii CMKP Szpital Bielański im. Ks. J. Popiełuszki ul. Cegłowska 80, 01-809 Warszawa tel.: +48 (22) 569-02-85 e-mail: tkrosny@gmail.com Artykuł Ocena zaburzeń ukrwienia u pacjentów z miażdżycowym niedokrwieniem kończyn dolnych za pomocą analizy nirs (spektroskopia w bliskiej podczerwieni) w Czytelni Medycznej Borgis. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Chcesz być na bieżąco? Polub nas na Facebooku: strona Wydawnictwa na Facebooku |








