Wydawca
|

|
ukazuje się od 1994 roku |
» Miejsce współczesnej endosonografii w diagnostyce obrazowej powikłań po operacjach koloproktologicznych© Borgis - Nowa Medycyna 3, s. 74-88
*Iwona Sudoł-Szopińska1, 2, Małgorzata Kołodziejczak2, Mariusz Furmanek3, Marek Szczepkowski4
Miejsce współczesnej endosonografii w diagnostyce obrazowej powikłań po operacjach koloproktologicznych
Value of anorectal endosonography in the diagnostics of complications following coloproctological surgery
1Zakład Diagnostyki Obrazowej, II Wydział Lekarski, Warszawski Uniwersytet Medyczny
Kierownik Zakładu: prof. dr hab. med. Wiesław Jakubowski 2Oddział Chirurgii Ogólnej z Pododdziałem Proktologii Szpitala na Solcu w Warszawie Ordynator Oddziału: dr n. med. Jacek Bierca Kierownik Proktologii: dr hab. n. med. Małgorzata Kołodziejczak 3Zakład Radiologii i Diagnostyki Obrazowej Centrum Medycznego Kształcenia Podyplomowego w Warszawie Kierownik Zakładu: prof. dr hab. med. Jerzy Walecki 4Oddział Chirurgii Ogólnej, Szpital Bielański, Warszawa Ordynator Oddziału: dr hab. med. Marek Szczepkowski Summary
This article presents the potential of modern imaging techniques (magnetic resonance, computer tomography and endosonography) in diagnosing complications of coloproctological operations. There was a special focus on endosonography, used routinely in our own proctological practice, and its value in diagnosing recurrent fistulas, poorly-draining anal abscesses, and damage to anal sphincters. In the case of recurrent fistulas, the endosonographic image is usually unambiguous and can well differentiate between post-operative scarring and recurrence of a fistula. If there would be any doubts, endosonography with contrast may be used. Further development brought 3D ultrasonography with various postprocessing techniques of the 3D data. Initial reports show that compared to traditional endosonography, the Volume Render Mode technique in B-mode grey scale is more sensitive in locating the internal opening of fistulas, differentiating scars from fistula recurrences, in diagnosing residual abscesses and injuries of anal sphincters. An examination using a 3D rectal probe placed in the immediate vicinity of the anus enables diagnosis of anal canal stenosis, even when its degree prevents a proper per rectum exam and full endosonographic evaluation (which would accurately assess the length and level of the stenosis and any concomitant changes in anal sphincters). Perineal ultrasonography is also important in the diagnosis of superficially located fistulas and anal abscesses, including recurrent ones, or fistulas coexisting with advanced changes like hidradenitis suppurativa, as well as in differentiating apocrine gland inflammation from anal fistulas, when the cutaneous presentation of hidradenitis suppurativa is not characteristic. Key words: coloproctological surgery complications, anorectal endosonography, recurrent anal fistula, anal sphincters incontinency
W diagnostyce powikłań po operacjach koloproktologicznych wykonywane są następujące rodzaje badań obrazowych: zdjęcie rentgenowskie przeglądowe jamy brzusznej, badanie USG jamy brzusznej, tomografia komputerowa (TK), rezonans magnetyczny (MR) z zastosowaniem cewki torso (miednicznej i/lub brzusznej) lub doodbytniczej (endoluminal MRI; EL-MRI) oraz badanie endosonograficzne kanału odbytu i odbytnicy (endoanal ultrasound; EAUS i endorectal ultrasound; ERUS). Rzadziej stosuje się fistulografię rentgenowską lub fistulografię TK.
Mimo że w Polsce dostępność tego badania jest nadal bardzo ograniczona, badanie MR, z uwagi na różnicowanie tkanek (wysoką rozdzielczość tkankową), wielopłaszczyznowość obrazowania i brak ekspozycji na promieniowanie jonizujące jest uznawane za metodę z wyboru do rozpoznawania powikłań w zakresie okrężnicy i odbytnicy, zwłaszcza u pacjentów, którzy wymagają częstych badań kontrolnych (1). Zastosowanie cewki doodbytniczej (w szczególności typu dedykowanego ocenie kanału odbytu) pozwala na szczegółową ocenę anatomiczną, jednak przy ograniczonym do 3-4 cm od światła kanału polu widzenia. Wprowadzenie cewki doodbytniczej jest także w wielu przypadkach powikłań zapalnych bolesne, wręcz niemożliwe. Z kolei badanie z zastosowaniem cewki torso umożliwia ocenę całej miednicy małej, ale cechuje się nieco mniejszą rozdzielczością przestrzenną w zakresie kanału odbytu i odbytnicy. W specjalistycznych ośrodkach wykonuje się także defekografię MR, pozwalającą na ocenę czynnościową dolnego odcinka przewodu pokarmowego.
W diagnostyce pooperacyjnych powikłań na poziomie kanału odbytu oraz odbytnicy badaniami o najwyższej skuteczności są EAUS/ERUS oraz EL-MRI lub MRI z cewką torso. Endosonografia jest wówczas badaniem pierwszego rzutu, z uwagi na możliwość szczegółowej oceny anatomicznej oraz satysfakcjonującą swoistość, a także fakt, iż jest dobrze tolerowana (może z wyjątkiem pacjentów ze szczeliną odbytu czy z silnym bólem w odbycie o innej etiologii), tańsza od innych badań obrazowych, i możliwa do wykonania w gabinecie lub przy łóżku chorego. Badanie MR jest uznawane za metodę z wyboru w przedoperacyjnej diagnostyce przetok nawrotowych, złożonych przetok odbytu i mnogich ropni, głównie u pacjentów z CD (2, 3). W praktyce jest wykonywane głównie w przypadku niejednoznacznego wyniku badania endosonograficznego.
TK jest uznawana za metodę mniej dokładną niż MR i endosonografia, szczególnie w ocenie powikłań w zakresie kanału odbytu i otaczających go tkanek, z uwagi na mniejszą rozdzielczość tkankową i wynikające stąd trudności z uwidocznieniem przetoki, zwłaszcza nie zawierającej treści płynowej lub gazu, na tle prawidłowych struktur odbytu. W przypadku drożnego ujścia zewnętrznego, możliwe jest podanie środka kontrastowego do przetoki, co ułatwia ocenę jej przebiegu względem zwieraczy odbytu. W celu różnicowania zmian zapalnych pod- z nadzzwieraczowymi potrzebne są rekonstrukcje obrazów TK w płaszczyźnie czołowej (wieńcowej); jakość tych rekonstrukcji w oparciu o starsze systemy TK klasyczne lub spiralne jednorzędowe nie jest satysfakcjonująca (4, 5, 6), co jednak nie dotyczy systemów spiralnych wielorzędowych pozwalających uzyskać warstwy wyjściowe o grubości 1 a nawet 0,5 mm (ryc. 1). Wówczas, TK jest z powodzeniem stosowana zwłaszcza u pacjentów z chorobą Leśniowskiego-Crohna, u których pozwala wykryć ropnie niedoszczętnie opróżnione, umożliwia zróżnicowanie ropni z zapaleniem tkanki podskórnej u osób z silnym bólem odbytu, wymagających znieczulenia do badania klinicznego, EAUS czy EL-MRI (3, 7, 8). TK pozwala także uwidocznić powikłania po operacjach wytworzenia zespolenia krętniczo-odbytniczego typu pauch, tj.: ropień (który może wymagać drenażu pod kontrolą badania USG lub TK), rozejście się zespolenia, zapalenie zbiornika jelitowego (na podstawie obecności pogrubiałej i ulegającej wzmocnieniu ściany), obecność przetoki w zespoleniu, zwężenie zespolenia, czy wreszcie powiększone węzły chłonne (1, 2).
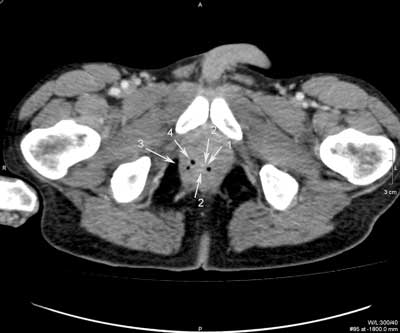
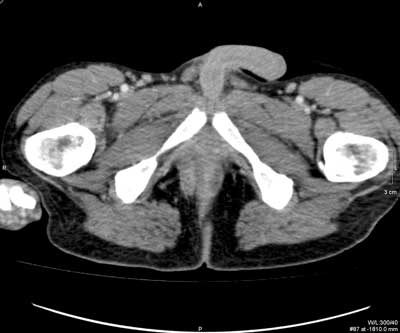
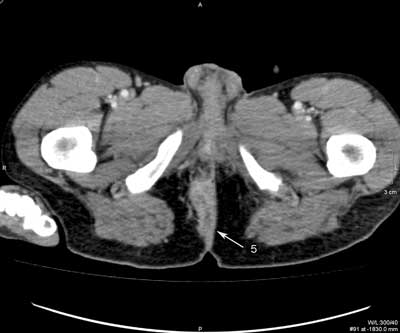
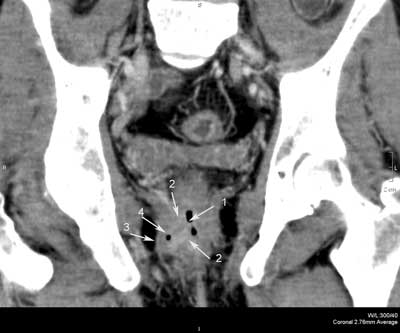 Ryc. 1. Badanie TK miednicy po dożylnym podaniu środka kontrastowego pod kątem nawrotowej przetoki przezzwieraczowej: obrazy w płaszczyźnie poprzecznej (a, b, c) oraz rekonstrukcja MPR w płaszczyźnie czołowej (d). Kanał przetoki uchodzący na godzinie 9.00 (1) identyfikują wzmacniające się ściany (2). Mikroropień w prawym dole kulszowo-odbytniczym (3) zawiera niewielką ilość treści płynowej oraz pęcherzyki gazu (4). Ujście zewnętrzne przetoki widoczne w szparze międzypośladkowej po stronie prawej (5).
W diagnostyce powikłań jw., nie można zapominać o przezbrzusznym badaniu USG, które umożliwia uwidocznienie wolnego płynu w jamie brzusznej, nieprawidłowych zbiorników, a wręcz miejsc nieszczelności zespoleń. W ośrodkach autorów jest ono badaniem pierwszego rzutu w diagnostyce powikłań pooperacyjnych, najbardziej, obok endosonografii, dostępnym.
W wielu przypadkach diagnostyki powikłań po operacjach koloproktologicznych, wynik badań obrazowych musi być interpretowany łącznie z innymi badaniami dodatkowymi, jak endoskopowym, manometrią anorektalną, badaniem elektromiograficznym EMG, rtg/MR lędźwiowo-krzyżowego odcinka kręgosłupa (pooperacyjna niewydolność zwieraczy). Manometria i EMG pozwalają na dokładną ocenę funkcji anorektalnych, w tym czucia w kanale odbytu. Jeśli ocena ta wypada niepomyślnie, należy bardzo poważnie brać pod uwagę możliwość pooperacyjnych powikłań dotyczących trzymania gazów i stolca.
Jak wspomniano, endosonografia, a obecnie trójwymiarowa endosonografia 3D EAUS/ERUS jest badaniem pierwszego rzutu w diagnostyce powikłań po operacjach proktologicznych. Jest ona w zasadzie wykonywana z dwóch wskazań: po pierwsze, u pacjentów objawowych, z podejrzeniem nawrotu przetoki lub nawrotu bądź niedostatecznie opróżniającego się ropnia odbytu, oraz po drugie, do oceny zwieraczy odbytu, w przypadku zgłaszanych objawów ich niewydolności (inkontynencji). W naszym ośrodku kontrolne badanie 3D EAUS jest rutynowo wykonywane 3 miesiące po operacji przetoki odbytu oraz po nacięciu skomplikowanego ropnia odbytu, w celu monitorowania opróżniania ropnia bądź rozpoznania nawrotu ropnia/przetoki odbytu. Istotnym celem kontroli pacjentów z ropniem jest także wczesne rozpoznanie wytworzenia się przetoki odbytu, często jeszcze niekompletnej.
W przypadku przetok nawrotowych obraz endosonograficzny jest z reguły jednoznaczny. Nasze ostatnie doświadczenia, podobnie jak innych autorów (9, 10), nie wykazują istotnej różnicy między dokładnością rozpoznawania w EAUS przetoki u osób z chorobą pierwotną i nawrotową; przetoka (pierwotna czy nawrotowa) częściej jest bardziej hipoechogeniczna niż blizna pooperacyjna, niejednokrotnie wręcz bezechowa, tak jak pisał Law i wsp. (11) (ryc. 2). Trudności w różnicowaniu pomiędzy zapalnym kanałem przetoki i blizną są jednak zgłaszane (11, 12, 13, 14) i po podaniu roztworu 3% wody utlenionej przez ujście zewnętrzne przetoki większość autorów zauważa poprawę dokładności EAUS ( hydrogen-peroxide ultrasound; HPUS) w tym zakresie (3, 12, 15, 16, 17). Jednak wartość endosonografii ze wzmocnieniem kontrastowym nadal nie jest satysfakcjonująca w stopniu pozwalającym uznać HPUS za metodę z wyboru do przedoperacyjnej diagnostyki przetoki nawrotowej (12). Skuteczność badania z kontrastem HPUS zależy bowiem od drożności przetoki i jej rozgałęzień w dniu badania oraz od ich wysokości/stosunku do zwieraczy odbytu. W sytuacji ich zwężenia, krętego przebiegu lub ziarninowania, wynik badania może nie być zadowalający i jest to generalnie podstawowa przyczyna rozbieżności w ocenie skuteczności metody badania kontrastowego w pracach różnych autorów. Jednocześnie korzyści z zastosowania kontrastu są widoczne głównie w przypadku przetok czy rozgałęzień niskich oraz, z oczywistych względów, jedynie tych przetok, które posiadają ujście zewnętrzne (którego, jak wiadomo, stosukowo często przetoki nawrotowe nie posiadają). W takich przypadku wskazaniem do operacji u osób objawowych będzie, w konfrontacji z badaniem proktologicznym, uwidocznienie w EAUS pasma hipoechogenicznego lub bezechowego. Natomiast taki obraz u osób bez objawów nawrotu i bez cech nawrotu w badaniu proktologicznym obliguje proktologa/chirurga do zlecenia kontrolnego badania EAUS za 3 miesiące, lub wcześniej w przypadku wystąpienia objawów.
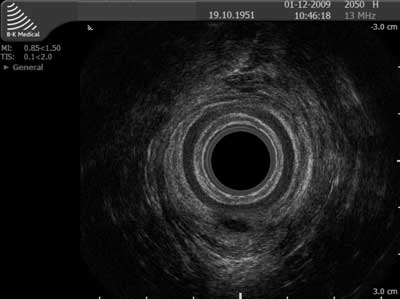
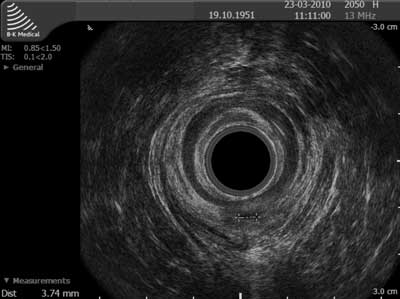 Ryc. 2. Badanie endosonograficzne nawrotowej przetoki odbytu: a) przetoka międzyzwieraczowa tylna prosta; b) nawrót przetoki 3 mies. po operacji jest w AES hipoechogeniczny, identycznie jak przetoka pierwotna (krzyżyki).
Przetokę z blizną można zróżnicować w badaniu MR. Sygnał z blizny w obrazach T1, T2 zależnych i w sekwencjach STIR jest niski, natomiast w świetle przetoki i w ropniu, z uwagi na obecność zmian zapalnych, w większości przypadków obserwuje się podwyższony sygnał w obrazach T2 zależnych i intensywne wzmocnienie ich ścian po dożylnym podaniu kontrastu (18-21) (ryc. 3, 4).
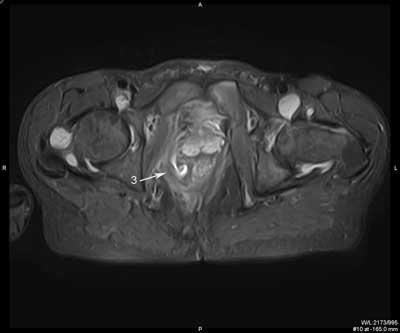
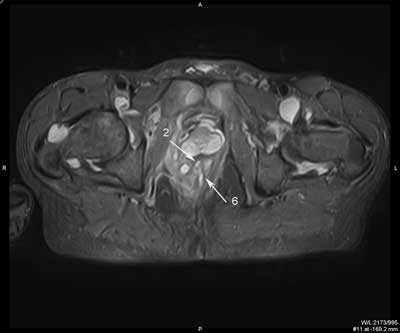
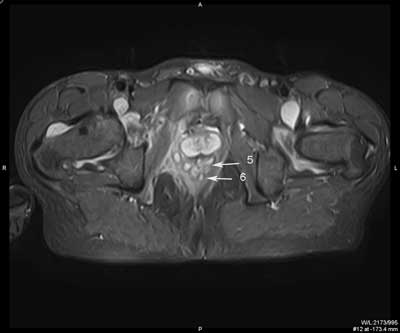
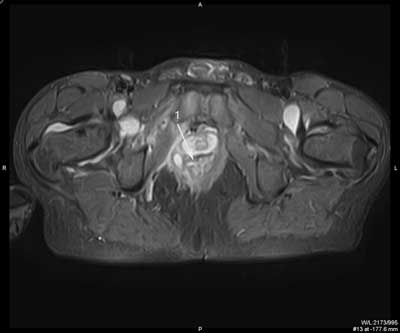
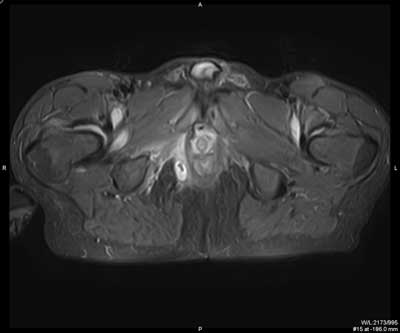
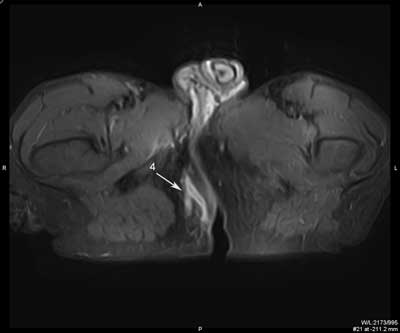
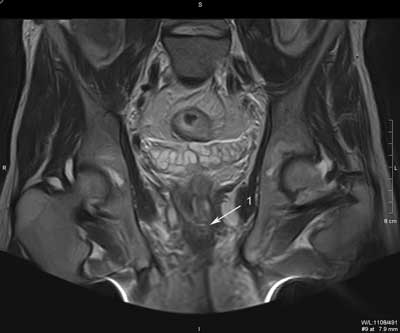
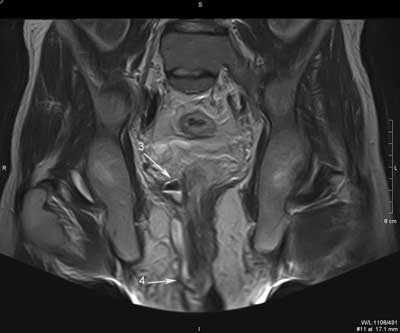 Ryc. 3. Badanie MR miednicy, obrazy STIR w płaszczyźnie poprzecznej (a, b, c, d, e, f) oraz obrazy T2 zależne w płaszczyźnie czołowej (g, h). Trzy nawrotowe przetoki odbytu u pacjenta z CD: mnoga i rozgałęziona przezzwieraczowa i dwie proste międzyzwieraczowe. Przetoka przezzwieraczowa posiada jedno ujście wewnętrzne na godzinie 9.00 (1), kolejne na godzinie 12.00 (2); kanał pionowy przebiega wzdłuż zewnętrznej powierzchni zwieracza zewnętrznego do góry, z wytworzeniem mikroropnia w przestrzeni naddźwigaczowej (3), a następnie do dołu; dystalnie rozgałęzia się (4) i uchodzi kilkoma ujściami zewnętrznymi w szparze międzypośladkowej i na prawym pośladku. Przetoki międzywieraczowe widoczne na godzinie 2.00 (5) i na godzinie 6.00; posiadają ujścia wewnętrzne (6).
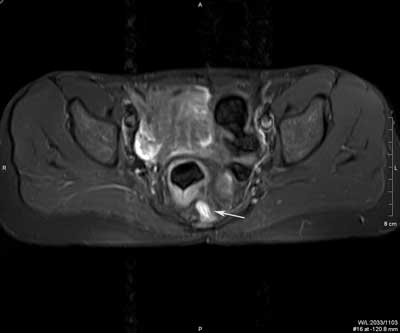
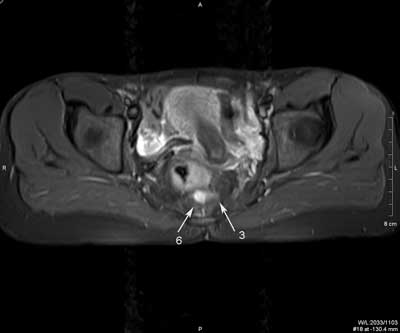

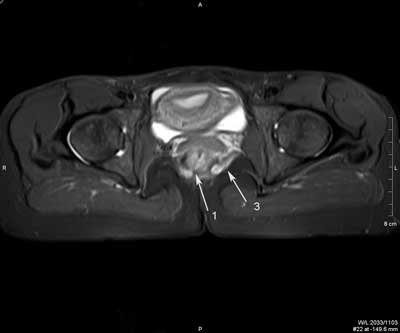
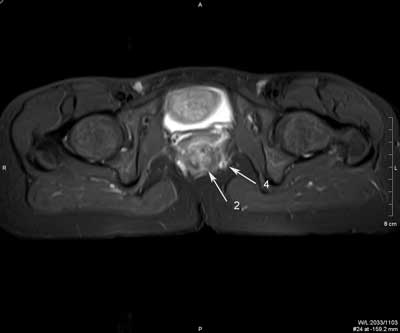
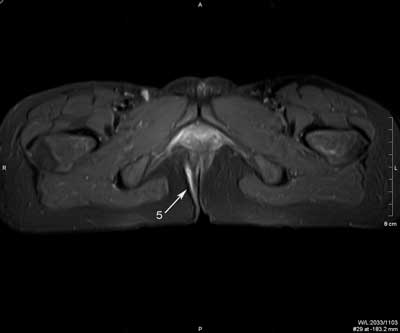
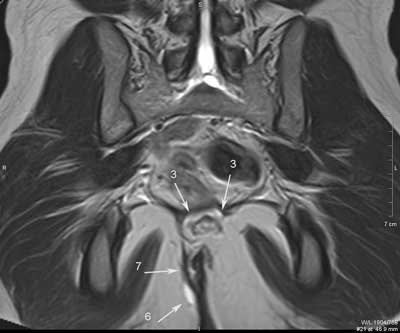
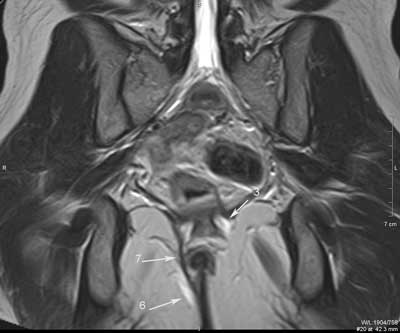 Ryc. 4. Badanie MR miednicy, obrazy STIR w płaszczyźnie poprzecznej (a, b, c, d, e, f) oraz obrazy T2 zależne w płaszczyźnie czołowej (g, h).
Nawrotowa, złożona, mnoga, wysoka przetoka przezzwieraczowa, z podkowiastym ślepym odgałęzieniem i kanałem penetrującym przedkrzyżowo u pacjentki z CD. Dwa ujścia wewnętrzne lokalizują się na godzinie 7.00 (1) i 6.00 (2). Podkowiaste odgałęzienie (3) ślepo zakończone w lewym dole kulszowo-odbytniczym (4). Ujście zewnętrzne w szparze międzypośladkowej po stronie prawej (5). Kolejne odgałęzienie kieruje się w stronę kości guzicznej i krzyżowej (6). W prawym dole kulszowo-odbytniczym widoczna blizna w sąsiedztwie przetoki po poprzedniej operacji (7). Użytecznym nowoczesnym narzędziem diagnostycznym jest obrazowanie endosonograficzne 3D wraz z różnymi technikami posprocessingu danych 3D. Chociaż ich wartość diagnostyczna nie została jeszcze ustalona, wstępne wyniki wskazują, że technika posprocessingu volume render mode (VRM) jest czulsza niż standardowe badanie w skali szarości B-mode w rozpoznawaniu położenia ujścia wewnętrznego przetoki (22). Co prawda, nasze wstępne badania tego nie potwierdzają, niemniej wskazują na istotną rolę techniki VRM w rozpoznawaniu resztkowych ropni, różnicowaniu blizn z nawrotem przetoki, i w diagnostyce urazów zwieraczy odbytu (ryc. 5, 6). Dzięki nowoczesnym technikom postprocessingu możliwa jest również, w badaniu głowicą rektalną 3D (3.3-10 MHz) przyłożoną do skóry bezpośrednio przy odbycie, diagnostyka zwężenia kanału odbytu w stopniu uniemożliwiającym badanie per rectum i endosonograficzne. Nasze pionierskie badania wykazały, że badanie to pozwala na dokładną przedoperacyjną ocenę morfologia zwężenia, tj. jego długości i poziomu, oraz współistniejących zmian w zwieraczach odbytu (ryc. 7).

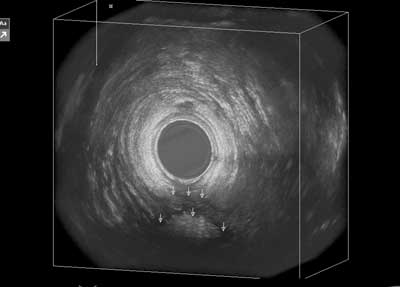 Ryc. 5. Badanie endosonograficzne z opcją Volume Render Mode. Resztkowy ropień zaodbytowy: a) przesłonięty przez cień od więzadła odbytowo-guzicznego w klasycznym badaniu 3D AES w skali czarno-białej; b) doskonale widoczny dzięki technice VRM.
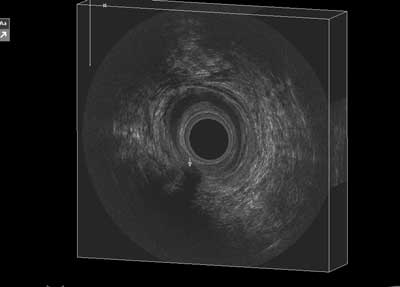
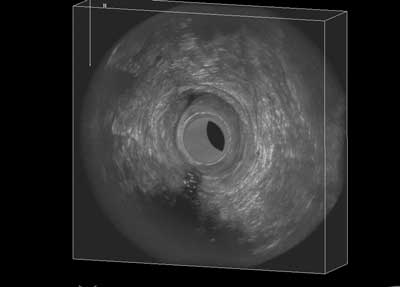 Ryc. 6. Badanie endosonograficzne. Nawrotowa przetoka przezzwieraczowa tylna, niska odbytu: a) wyjściowe badanie 3D AES; b) dzięki technice VRM w sposób spektakularny uwidacznia się płynowa zawartość drożnego kanału przetoki.
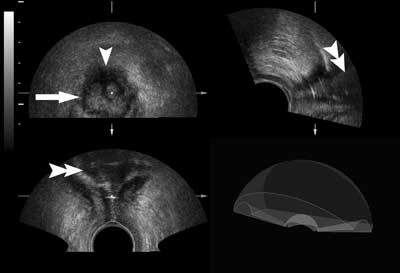 Ryc. 7. Badanie przezkroczowe głowicą endosonografczną 3D. Dużego stopnia zwężenie kanału odbytu po operacjach na kanale odbytu: rekonstrukcja obrazu „do przodu” od głowicy endorektalnej 3D przyłożonej od odbytu obrazuje zwężony kanał odbytu w trzech płaszczyznach.
Koniecznym uzupełnieniem endosonograficznej oceny kanału odbytu jest, w naszej opinii, badanie przezkroczowe USG ( transperineal ultrasound; TPUS), nie stosowane powszechnie w większości ośrodków. Zawsze wykonujemy je w diagnostyce powierzchownie przebiegających przetok i ropni odbytu, w tym nawrotowych, ponadto w celu wykluczenia przetoki współistniejącej z zaawansowanymi zmianami typu hidradenitis suppurativa, bądź pod kątem różnicowania zapalenia gruczołów apokrynowych z przetoką odbytu, gdy zmiany skórne w hidradenitis suppurativa nie są charakterystyczne (ryc. 8). Są to przypadki często wielokrotnie operowane z powodu podejrzewanej przetoki lub ropnia odbytu. TPUS potwierdza typową podskórną lokalizację zmian. W ocenie podskórnie czy powierzchownie przebiegającej przetoki nawrotowej TPUS pozwala dokładnie określić głębokość położenia ujścia wewnętrznego (ryc. 9), zlokalizować podskórne odgałęzienia do krocza, podstawy moszny, itp., których nie można ocenić w EAUS. Nawrót przetoki można albo uwidocznić w postaci typowego pasma hipoechogenicznego, bądź zwiastunem jego jest stan zapalny tkanek, widoczny w badaniu dopplerowskim.
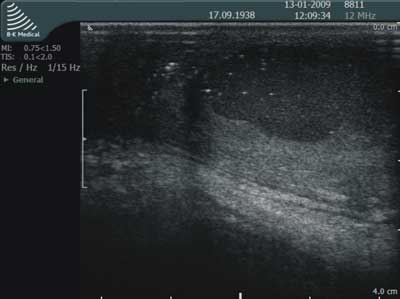
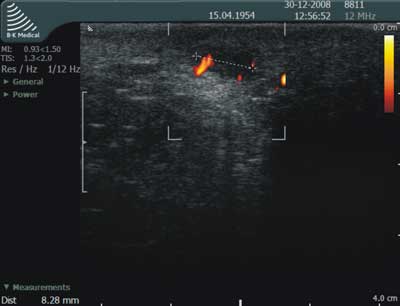 Ryc. 8. Badanie USG przezkroczowe wykonane głowicą liniową: a) zaawansowane i b) mało zaawansowane zmiany w przebiegu choroby Verney'a.
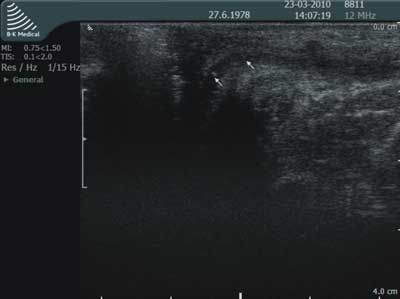 Ryc. 9. Badanie USG przezkroczowe: ujście wewnętrzne płytkiej przetoki przezzwieraczowej.
Pozostaje jeszcze problem pooperacyjnej inkontynencji. EAUS jest metodą z wyboru do uwidaczniania urazów morfologicznych zwieraczy odbytu (23, 24, 25). Jest wykonywana w celu różnicowania pacjentów z objawami inkontynencji z prawidłowym obrazem zwieraczy oraz z uszkodzeniami. Umożliwia wówczas precyzyjne określenie rozległości uszkodzenia, konieczne w kwalifikacji pacjenta do operacji i w jej planowaniu. Po operacjach przetoki często obserwuje się blizny w zwieraczu zewnętrznym lub w mięśniu łonowo-odbytniczym, czy ubytek zwieracza wewnętrznego, związany z jego częściowym wycięciem w trakcie usuwania przetoki. Podobny zresztą ogniskowy ubytek ciągłości zwieracza wewnętrznego jest obserwowany często po sfinkterotomii wewnętrznej wykonywanej w przebiegu leczenia szczeliny odbytu, co jest wiązane z następowym nietrzymaniem gazów i brudzeniem (26). Oczywiście sam obraz EAUS nie pozwala rozpoznać, czy uwidocznione morfologiczne uszkodzenie zwieracza wewnętrznego jest rzeczywiście odpowiedzialne za zgłaszane objawy inkontynencji. Wynik przedoperacyjnego badania proktologicznego oraz zintegrowana ocena obrazu zwieracza w EAUS i jego funkcji w manometrii odbytowo-odbytniczej pozwoli na zróżnicowanie uszkodzenia morfologicznego z neurogennym (ryc. 10).
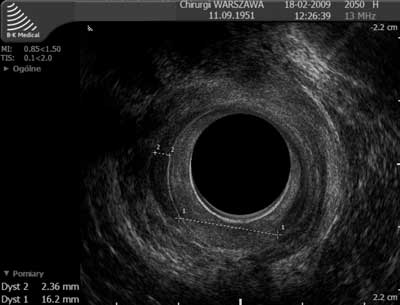

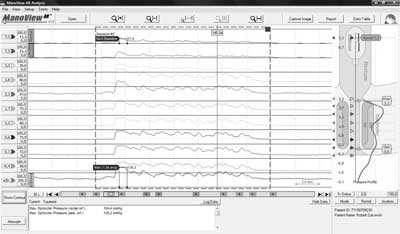 Ryc. 10. Ocena morfologiczna i czynnościowa zwieraczy odbytu u pacjentki z objawami brudzenia po operacji szczeliny odbytu: a) w endosonografii ogniskowy ubytek zwieracza wewnętrznego na tylnym obwodzie typowy dla sfinkterotomii otwartej; b) w manometrii anorektalnej obniżone ciśnienie spoczynkowe przy zachowanej sile skurczu dowolnego. Piśmiennictwo
1. Broder JC et al.: Ileal pouch-anal anastomosis surgery: imaging and intervention for post-operative complications. Radiographics 2010; 30(1): 221-33. 2. Alexander F: Complications of ileal pouch anal anastomosis. Semin Pediatr Surg 2007; 16(3): 200-4. 3. Halligan S, Stoker J: Imaging of fistula in ano. Radiology 2006; 239: 18-33. 4. Halligan S: Review imaging fistula-in-ano. Clinical Radiol 1998; 53: 85-95. 5. Schratter-Sehn AU et al.: Endoscopic ultrasonography versus computed tomography in the differential diagnosis of perianorectal complications in Crohn's disease. Endoscopy 1993; 25: 582-586. 6. Schratter-Sehn AU et al.: Endoscopic features of the lower pelvic region in Crohn's disease. Am J Gastro 1994; 88: 1054-1057. 7. Guillaumin E et al.: Perirectal inflammatory disease: CT findings. Radiology 1986; 161: 153-157. 8. Yousem DM, Fishman EK, Jones B: Crohn disease:perirectal and perianal findings at CT. Radiology 1988; 167: 331-334. 9. Deen KI et al.: Fistulas in ano: endoanal ultrasonographic assessment assists decision making for surgery. Gut 1994; 35: 391-394. 10. Fernández-Frías AM et al.: Is anal endosonography useful in the study of recurrent complex fistula-in-ano? Rev Esp Enferm Dig 2006; 98(8): 573-81. 11. Law PJ, Talbot RW, Bartram CI, Northover JMA: Anal endosonography in the evaluation of perianal sepsis and fistula in ano. Br J Surg 1989; 76: 752-755. 12. Santoro GA, Ratto C: Accuracy and reliablity of endoanal ultrasonography in the evaluation of perianal abscesses and fistula-in-ano. In: Santoro GA, Di Falco G (ed) Benign anorectal diseases. Diagnosis with endoanal and endorwectal ultrasound and new treatment options. Springer-Verlag Italy Milan 2006; pp 141-183. 13. Choen S, Nicholls RJ: Anal fistula. Br J Surg 1992; 79: 197-205. 14. Cheong DMO et al.: Anal endosonography for recurrent anal fistulas:image enhancement with hydrogen peroxide. Dis Colon Rectum 1993; 36: 1158-60. 15. Kruskal JB, Kane RA, Morrin MM: Peroxide-enhanced anal endosonography: technique, image interpretation, and clinical applications. Radiographic 2001; 21: 51-73. 16. Ratto C et al.: How can the assessment of fistula in ano be improved? Dis Colon Rectum 2000; 43: 1375-82. 17. Sudoł-Szopińska I et al.: Usefulness of the hydrogen peroxide enhancement in the diagnosis of the anal and ano-vaginal fistulas. Eur Radiol 2003; 13: 1080-1084. 18. Stoker J et al.: Endoluminal MR imaging of the rectum and anus: technique, applications, and pit-falls. RadioGraphics 1999; 19: 383-398. 19. Ziech M, Felt-Bersma R, Stoker J: Imaging of perianal fistulas. Clin Gastroenterol Hepatol 2009; 7(10): 1037-45. 20. Sabir N, Sungurtekin U, Erdem E, Nessar M: Magnetic resonance imaging with rectal Gd-DTPA: new tool for the diagnosis of perianal fistula. Int J Colorectal Dis 2000; 15(5-6): 317-22. 21. Stoker J, Rociu E, Wiersma TG, Laméris JS: Imaging of anorectal disease. Br J Surg 2000; 87(1): 10-27. 22. Santoro GA, Fortling B: The advantages of volume rendering in three-dimensional endosonography of the anorectum. Dis Colon Rectum 2006; 50: 359-368. 23. Bartram CI: Anal sphincter disorders. Gastrointestinal Endoscopy 1996; 43: 32-34. 24. Hill MC, Rifkin MD, Tessler FN: Ultrasound evaluation of the anal sphincter in fecal incontinence. Ultrasound Quarterly 1998; 14: 209-217. 25. Yee LF et al.: Use of endoanal ultrasound in patients with rectovaginal fistulas. Dis Colon Rectum 1999; 42: 1057-1064. 26. Ratto C: Invited Commerntary. Surgical and endosonographic anatomy of the rectum. In: Santoro GA, Di Falco G (ed) Atlas of endoanal and endorectal ultrasonography. Springer-Verlag Italy Milan 2004; pp 42-48.
otrzymano/received: 2010-08-04 zaakceptowano/accepted: 2010-09-06 Adres/address: *Iwona Sudoł-Szopińska Zakład Diagnostyki Obrazowej, II Wydział Lekarski, Warszawski Uniwersytet Medyczny ul. Kondratowicza 8, 03-242 Warszawa tel.: (71) 784-12-59 e-mail: sudolszopinska@gmail.com Artykułu Miejsce współczesnej endosonografii w diagnostyce obrazowej powikłań po operacjach koloproktologicznych w Czytelni Medycznej Borgis. |